| Afaceri | Agricultura | Comunicare | Constructii | Contabilitate | Contracte |
| Economie | Finante | Management | Marketing | Transporturi |
Agricultura
|
|
Qdidactic » bani & cariera » agricultura Proprietatile chimice ale solurilor |
Proprietatile chimice ale solurilor
Proprietatile chimice ale solurilor
1. Solutia solului si proprietatile acesteia
Solutia solului reprezinta apa din sol incarcata cu diferite substante minerale si organice aflate in stare de dispersie ionica, moleculara sau coloidala, ce poate avea concentratii diferite in functie de natura solului, umiditate, continut in substante nutritive, etc.
Principalii compusi intalniti in solutia solului sunt:
saruri de Ca, Mg, K, Na, NH4, etc;
saruri ale acidului azotic, clorhidric, sulfuric, carbonic, fosforic etc;
compusi ai fierului, manganului, aluminiului etc.;
amoniac, CO2;
acizi organici: aminoacizi, acizi humici, acid acetic, oxalic etc.
Raportul dintre substantele minerale si organice din solutia solului poate fi aproximativ egal (soluri din zone putin umede), in favoarea celor organice (soluri din zonele umede) sau in favoarea celor minerale (soluri din zonele aride sau semiaride).
Solutia solului are o alcatuire complexa, cea mai mare parte a compusilor chimici (saruri, acizi etc.) sunt prezenti in solutie sub forma disociata: Ca++, Mg++, Na+, K+, NO-, SO2-, OH-, PO3- etc.
Compozitia si concentratia solutiei solului poate varia de la un sol la altul cat si la acelasi sol in functie de urmatorii factori:
continut in humus sau alte substante organice;
gradul de solubilitate si natura substantelor minerale;
activitatea microorganismelor si a plantelor;
complexul coloidal;
cantitatea de apa din sol;
masurile agrotehnice, agrochimice si ameliorative aplicate.
2. Coloizii solului si proprietatile lor
|
Datorita diversitatii acestora, coloizii solului se impart in trei grupe: minerali, organici si organo-minerali.
Coloizii minerali sunt reprezentati de argila, oxizi si hidroxizi de fier si aluminiu, silice coloidala, coloizii organici sunt reprezentati de acizii humici, hidrati de carbon, proteine etc., iar cei organo-minerali de compusii acizilor humici si ai altor compusi organici cu elementele chimice si compusii minerali (humati, argilo-humine, fero-humati etc.).
Importanta si ponderea coloizilor in sol este urmatoarea: argila, humus, oxizi si hidroxizi de Fe si Al, silice coloidala etc.
Cationii adsorbiti de complexul coloidal pot fi schimbati de catre alti cationi din solutia solului datorita posibilitatii de trecere a cationilor din complexul coloidal in solutie si invers, fenomen cunoscut sub numele de schimb de cationi.
Fenomenul de adsorbtie cationica a scos in evidenta faptul ca schimbul cationic se desfasoara dupa anumite reguli sau legi.
Legea echivalentei - schimbul cationic, are loc in proportii echivalente (proportia cationilor ce trec din complex in solutie este echivalenta cu cea a cationilor ce trec din solutie in complex.). Conform acestei legi, se pot calcula dozele de amendamente calcaroase sau fosfatice.
Legea reversibilitatii - fenomenul de schimb cationic este reversibil (cationii adsorbiti de complexul coloidal sunt inlocuiti de alti cationi din solutie. Schimbul este reversibil, trecerea cationilor fiind continua.
Legea echilibrului - ca orice reactie reversibila, schimbul cationic are loc pana la stabilirea unui echilibru intre complexul coloidal si solutia solului, echilibru ce se realizeaza instantaneu.
Legea energiei de adsorbtie - energia de adsorbtie a cationilor precum si energia de deplasare a cationilor din complex in solutie este diferita si variaza in functie de valenta si gradul de hidratare a cationilor.
![]() Na+,
K+, Mg++, Ca++, Al+++, H+
Na+,
K+, Mg++, Ca++, Al+++, H+
creste energia de adsorbtie
3. Indicii ce caracterizeaza capacitatea de schimb cationic
Principalii indici care caracterizeaza capacitatea de schimb cationic sunt: capacitatea de schimb pentru baze, capacitatea de schimb pentru hidrogen, capacitatea totala de schimb cationic, gradul de saturatie in baze.
. capacitatea de schimb pentru baze (SB) - reprezinta suma cationilor bazici (Ca, Mg, Na, K) adsorbiti in complex, care se exprima in m.e. ./100 g sol.
. capacitatea de schimb pentru hidrogen (SH) - reprezinta suma cationilor de H+ si se exprima in m.e. ./100 g sol.
. capacitatea totala de schimb cationic (T) - reprezinta capacitatea totala a cationilor adsorbiti in complex si se exprima in m.e. ./100 g sol.
T = SB + SH
. gradul de saturatie in baze (V) - gradul in care complexul coloidal este saturat cu cationi bazici.
V = ![]()
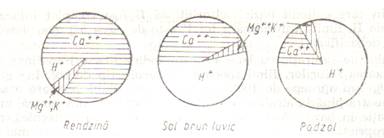
Solurile care nu au H+ adsorbiti in complex - T = SB, iar cele care au H+ adsorbiti in complex, V < 100. Gradul de saturatie in baze este specific fiecarui tip de sol care se poate corela cu pH - ul solului; cu cat scade V%, scade si pH-ul.
4. Reactia solului
- rol important in caracterizarea solurilor si pentru practica agricola;
- influenteaza activitatea microorganismelor din sol;
- influenteaza atat vegetatia spontana cat si cea cultivata;
- creste presiunea osmotica influentand concentratia solutiei solului;
- alegerea sortimentului de culturi prin cerintele fiecarei plante;
- rol important in aplicarea ingrasamintelor chimice cu reactie fiziologica acida sau alcalina etc.
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2024 - Toate drepturile rezervate -| |
|
|
|||||
|
|||||
|
|||||
Referate pe aceeasi tema | |||||
|
| |||||
|
|||||
|
|
|||||