
| Biologie | Botanica | Chimie | Didactica | Fizica | Geografie |
| Gradinita | Literatura | Matematica |
Chimie
|
|
Qdidactic » didactica & scoala » chimie Chimia alimentara - indrumar metodic |
Chimia alimentara - indrumar metodic
UNIVERSITATEA TEHNICA A MOLDOVEI
Facultatea Tehnologie si Management
in Industria Alimentara
CATEDRA TEHNOLOGIA CONSERVARII
CHIMIA ALIMENTARA
INDRUMAR METODIC
pentru studentii specialitatilor:
541.1 - Tehnologia si Managementul Alimentatiei Publice
Tehnologia produselor alimentare
552.2 - Biotehnologii industriale
Indrumarul metodic este destinat studentilor de la specialitatile: 541.1 - Tehnologia si Managementul Alimentatiei Publice; 541.2 - Tehnologia produselor alimentare; 552.2 - Biotehnologii industriale a Facultatii de Tehnologie si Management in Industria Alimentara. In indrumar sunt incluse continutul prelegerilor, seminarelor, lucrarile de laborator, chestionarul pentru examene, lucrarile de control pentru studentii cu frecventa redusa.
CHIMIA ALIMENTARA
CHIMIA ALIMENTARA
I. PROGRAMA ANALITICA
Activitatea didactica
|
Activitati |
Specialitatile: 552.2 |
Specialitatea: |
||
|
Sem. 5 |
Sem. |
Sem. 4 |
Sem. |
|
|
sectia zi |
frecventa redusa |
sectia zi |
frecventa redusa |
|
|
Prelegeri |
|
|
|
|
|
Seminare |
|
|
|
|
|
Lucrari de laborator |
|
|
|
|
|
Total ore pe semestru |
|
|
|
|
|
Lucrari de verificare |
|
|
|
|
|
Atestari |
|
|
|
|
|
Examen |
|
|
|
|
|
Numarul de credite |
|
|
|
|
Scopul si obiectivele disciplinei
Scopul disciplinei este: studiul compozitiei chimice, proprietatilor nutritive si senzoriale ale alimentelor; studiul proprietatilor functionale ale compusilor chimici; modificarea lor atat in fluxul tehnologic de obtinere a alimentelor cat si pe parcursul pastrarii; studierea proprietatilor fizico-chimice si functionale ale aditivilor alimentari.
Chimia alimentara este o disciplina din stiintele chimice, care include si elementele de baza ale biochimiei, chimiei fizice, chimiei organice, microbiologiei, tehnologiilor produselor alimentare, Biotehnologiei; include acte normative ale comitetului international "Codex Alimentarius".
Obiectivele de baza ale disciplinei sunt studierea:
caracteristicii generale a produselor alimentare;
proprietatilor fizico-chimice si functionale ale apei, glucidelor, proteinelor si ale lipidelor;
modificarilor chimice si fizico-chimice ai compusilor chimici in compozitii alimentare;
substantelor biologic active a alimentelor;
utilizarii aditivilor alimentari in obtinerea alimentelor.
Sarcinile studierii cursului prevad:
acumularea cunostintelor despre proprietatile si caracteristicile alimentelor;
utilizarea cunostintelor "chimiei alimentare" in insusirea metodelor si tehnologiilor de obtinere a alimentelor cu proprietati planificate;
cunoasterea modificarilor chimice a compusilor in compozitii alimentare, influenta lor asupra calitatii alimentelor.
Studentii trebuie sa posede:
cunostinte despre influenta compusilor chimici asupra valorii nutritive si proprietatilor senzoriale ale alimentelor;
aplicarea cunostintelor in rezolvarea problemelor tehnologice de obtinere a alimentelor, evolutia calitatii produselor finite.
1. 2. Continutul prelegerilor
Specialitatile: 541.1; 541.2; 5
|
Nr. temei |
Temele prelegerilor |
Nr. de ore |
|
|
Sectia zi |
Sectia cu frecventa redusa |
||
|
|
|
|
|
|
|
Caracteristica generala a produselor alimentare. Compozitia chimica a alimentelor. Valoarea nutritiva a alimentelor. Proprietatile senzoriale ale alimentelor. |
|
|
|
|
Apa in produsele alimentare. Structura si proprietatile fizico-chimice ale apei. Activitatea apei. Influenta activitatii apei asupra reactiilor chimice si biochimice in alimente. Interactiuni hidrofobe. Activitatea apei alimentelor. |
|
|
|
|
Proprietatile fizico-chimice si functionale ale glucidelor Glucide in produse alimentare. Proprietatile fizico-chimice si functionale ale mono - dizaharidelor si polizaharidelor. Modificarea chimica a glucidelor, degradarea termica, caramelizarea. Proprietatile functionale ale amidonului si ale substantelor pectice. Fibrele alimentare. |
|
|
|
|
|
|
|
|
|
Proprietatile fizico-chimice si functionale ale proteinelor. Proprietatile fizico-chimice ale aminoacizilor. Clasificarea proteinelor. Hidratarea interactiunii hidrofobe, denaturarea proteinelor. Proprietatile functionale ale proteinelor. Activitatea chimica a proteinelor. Reactia lui Maillard. Reactia lui Strecker. Valoarea nutritiva a proteinelor. |
|
|
|
|
Proprietatile fizico-chimice si functionale ale lipidelor. Structura si proprietatile fizico-chimice a lipidelor. Acizii grasi, gliceride, lipide complexe. Proprietatile functionale a lipidelor. Interactiuni hidrofobe. Structura alimentelor de tip A/L si L/A. Modificarea lipidelor prin hidroliza, degradarea oxidativa si degradarea termica. Influenta lipidelor asupra calitatii alimentelor. |
|
|
|
|
Proprietatile fizico-chimice si functionale ale acizilor organici. Caracteristica acizilor organici. Proprietatile senzoriale. Influenta acizilor organici asupra modificarilor chimici a compusilor alimentelor. |
|
|
|
|
|
|
|
|
|
Procesele de oxidare a alimentelor. Implicarea oxigenului in procesele de oxidare a compusilor chimici. Oxidarea lipidelor. Degradarea oxidativa a substantelor biologic active: acid ascorbic, polifenolilor, antocianelor. Reactii in lant, formarea radicalilor liberi. Bioantioxidanti. Proprietatile functionale ale bioantioxidantilor. |
|
|
|
|
Aditivii alimentari. Clasificarea. Utilizarea aditivilor alimentari. Codex Alimentarius, documente normative. Caracteristica proprietatilor fizico-chimice si functionale a aditivilor alimentari: coloranti, conservanti, antioxidanti gelificanti, emulgatori, aditivi de corectare a gustului alimentelor, antispumanti, stabilizatori ai structurii alimentelor. Principiile de utilizare a aditivilor alimentari in tehnologiile de fabricare a produselor alimentare. |
|
|
|
|
Total ore: |
|
|
1.3. Continutul seminarelor
|
Nr.teme |
Temele |
Volum, ore |
|||||
|
Sectia zi |
Sectia. cu frecventa. redusa |
||||||
|
|
|
|
|
||||
|
|
Macro- si micronutrienti. Xenobiotici. Indicii proprietatilor senzoriale a alimentelor. |
|
|
||||
|
|
Activitatea apei. Curbele de sorbtie si desorbtie a apei. |
|
|
||||
|
|
Proprietatile functionale ale glucozei, fructozei, zaharozei si lactozei. |
|
|
||||
|
|
Proprietatile functionale ale amidonului si pectinei. Fibrele alimentare. |
|
|
||||
|
|
Proteinele: hidratarea, denaturarea, hidroliza. Proprietatile functionale ale proteinelor |
|
|
||||
|
|
Reactia lui Maillard. Valoarea nutritiva a proteinelor. |
|
|
||||
|
|
Structura lipidelor. Interactiuni hidrofobe de tip L/A, A/L. |
|
|
||||
|
|
Oxidarea lipidelor. |
|
|
||||
|
|
Degradarea oxidativa a acidului ascorbic, a polifenolilor, antocianelor, carotenelor. |
|
|
||||
|
|
Proprietatile fizico-chimice si functionale ale aditivilor alimentari. |
|
|
||||
|
|
Total ore: |
|
|
||||
1.4. Continutul lucrarilor de laborator
|
Nr. |
Denumirea lucrarii de laborator |
Specialitatile |
||||
|
552.2 |
|
|||||
|
Volum, ore |
||||||
|
Sectia |
Sectia |
|||||
|
zi |
cu frecventa redusa |
zi |
cu frecventa redusa |
|||
|
|
Determinarea cantitatii de apa legata in produse vegetale. |
|
|
|
|
|
|
|
Determinarea 5- OMF in produse alimentare tratate termic. |
|
|
|
|
|
|
|
Identificarea colorantilor naturali si sintetici in produsele alimentare. |
|
|
|
|
|
|
|
Determinarea gradului de esterificare a substantelor pectine. |
|
|
|
|
|
|
|
Metodele de identificare a proteinelor. |
|
|
|
|
|
|
|
Determinarea indicelui de peroxid al lipidelor. |
|
|
|
|
|
|
|
Proprietatile functionale ale aditivilor alimentari. |
|
|
|
|
|
|
|
Total ore: |
|
|
|
|
|
1.5. Subiecte pentru examene
- Caracteristica generala a compozitiei chimice a alimentelor.
- Caracteristica macronutrimentilor.
- Caracteristica micronutrimentilor.
- Proprietatile senzoriale ale alimentelor. Gust, miros, aspect.
- Valoarea nutritiva a alimentelor.
- Valoarea energetica a alimentelor.
- Fenomene de hidratare si interactiuni hidrofobe.
- Formele apei legate in alimente.
- Activitatea apei.
- Influenta activitatii apei asupra reactiilor chimice si biochimice.
- Stabilitatea alimentelor in functie de valoarea activitatii apei.
- Proprietatile functionale a mono- si dizaharidelor.
- Amidonul. Structura, proprietatile functionale.
- Hidroliza amidonului.
- Structura si proprietatile functionale a substantelor pectice.
- Mecanismul de gelificare pe baza pectinei slab metoxilate si puternic metoxilate.
- Indice pentru aprecierea gustului dulce.
- Caramelizarea glucidelor. Formarea culorii brune.
- Prevenirea proceselor de caramelizare..
- Mecanismul formarii 5-OMF.
- Fibrele alimentare, caracteristica, proprietatile.
- Caracteristica aminoacizilor.
- Proprietatile proteinelor in functie de continutul aminoacizilor polari in structura macromoleculelor.
- Proprietatile proteinelor denaturate.
- Influenta pH asupra capacitatii de legare a apei de proteine.
- Caracteristica generala a reactiei intre proteine si glucide (reactia lui Maillard).
- Etapele principale a reactiei lui Maillard.
- Reactia lui Strecкer.
- Degradarea si descompunerea proteinelor.
- Caracteristica acizilor grasi saturati si nesaturati.
- Proprietatile functionale a lipidelor.
- Degradarea termica a lipidelor.
- Hidroliza trigliceridelor.
- Proprietatile fizico-chimice a acizilor organici.
- Clasificarea substantelor biologic active in alimente.
- Proprietatile si modificarea clorofilei, carotenelor, antocianelor, polifenolilor.
- Oxidarea lipidelor. Reactii in lant.
- Formarea radicalilor liberi in procesul de oxidare.
- Metodele de prevenire a proceselor de oxidare.
- Modificarile oxidative a acidului ascorbic.
- Antioxidanti. Clasificarea. Caracteristica generala.
- Mecanismul activitatii chimice a antioxidantilor.
- Aditivii alimentari. Caracteristica, clasificarea.
- Proprietatile functionale si caracteristica:
aditivii de structura;
aditivii de gust;
aditivii de aspect;
conservantii chimici;
cercetarea valorii pH;
antioxidanti sintetici;
aditivii de gust dulce.
- . Activitatea comitetului "Codex Alimentarius".
- Inofensivitatea produselor alimentare.
1.6. Lucrari de control pentru studentii cu frecventa redusa
Varianta 1
- Activitatea apei. Dependenta stabilitatii alimentelor de valoarea activitatii apei.
- Proprietatile functionale ale lipidelor.
- Substante sintetice cu gust dulce. Caracteristica.
Varianta 2
- Procesul de caramelizare a mono- si dizaharidelor.
- Proprietatile functionale ale proteinelor.
- Caracteristica aditivilor de structura.
Varianta 3
- Reactiile chimice a oxidarii lipidelor. (Reactii in lant).
- Proprietatile functionale ale amidonului.
- Conservanti chimici. Caracteristica.
Varianta 4
- Procesul de denaturare a proteinelor.
- Proprietatile functionale a acizilor grasi saturati.
- Antioxidanti naturali. Caracteristica.
Varianta 5
- Influenta activitatii apei asupra cineticei reactiilor chimice.
- Proprietatile functionale ale zaharozei.
- Emulgatori. Caracteristica.
Varianta 6
- Degradarea termica a lipidelor.
- Metodele de prevenire a reactiilor de imbrunare a alimentelor.
- Colorantii naturali (pigmentii) a alimentelor. Caracteristica.
Varianta 7
- Reactia lui Maillard. Etapele principale ale reactiei.
- Proprietatile functionale ale substantelor pectice.
- Gelifianti. Caracteristica.
Varianta 8
- Reactiile formarii 5-OMF.
- Proprietatile functionale ale polizaharidelor.
- Clasificarea aditivilor alimentari.
Varianta 9
- Metodele de prevenire a procesului de oxidare a lipidelor.
- Valoarea nutritiva si energetica a alimentelor.
- Substantele naturale si sintetice cu gust dulce. Caracteristica.
Varianta 10
1. Caracteristica aminoacizilor in alimente.
2. Influenta apei asupra stabilitatii alimentelor.
3. Utilizarea conservantilor in industria alimentara.
II. SEMINARE
Seminarul I
Tema: Caracteristica generala a produselor alimentare (2ore)
Subiectele:
Compozitia chimica a produselor alimentare:
macronutrienti (glucide, proteine, lipide);
micronutrienti (microelementele, vitaminele, substantele minerale);
substante secundare (substante straine, substante toxice, fibre alimentare);
2.Proprietatile senzoriale ale alimentelor:
senzatii gustative;
senzatii olfactive;
senzatii optice;
senzatii tactile;
senzatii acustice
3. Activitatea apei. Curbele de sorbtie si desorbtie a apei.
Seminarul II
Tema: Proprietatile fizico-chimice si functionale ale glucidelor (2ore)
Subiectele:
Proprietatile functionale ale glucidelor:
glucozei,
fructozei,
zaharozei,
lactozei.
2 .Modificarea chimica a glucidelor, degradarea termica, caramelizarea.
3. Proprietatile functionale ale amidonului si pectinei.
Seminarul III
Tema: Fibrele alimentare. (1ora)
Proteinele. Aminoacizii (1ore)
Subiectele:
- Proprietatile functionale ale fibrelor alimentare.
- Proteinele:
clasificarea proteinelor;
proprietatile functionale ale proteinelor, hidratarea, denaturarea, hidroliza.
3. Proprietatile fizico-chimice ale aminoacizilor.
Seminarul IV
Tema: Proteinele. (2ore)
Subiectele:
- Caracteristica proteinelor.
- Reactia lui Maillard
- Valoarea nutritiva a proteinelor.
Seminarul V
Tema: Proprietatile fizico-chimice si functionale a lipidelor (2ore)
Subiectele:
Structura si proprietatile fizico-chimice a lipidelor
- Interactiuni hidrofobe de tip L/A, A/L.
- Modificarea lipidelor prin hidroliza, degradarea oxidativa si degradarea termica
4.Proprietatile fizico-chimice si functionale a acizilor organici.
Seminarul VI
Tema: Substantele biologic active (2ore)
Subiectele:
1. Degradarea oxidativa a substantelor biologic active:
acidului ascorbic,
polifenolilor,
antocianelor,
carotenoizilor.
2. Reactii in lant, formarea radicalilor liberi.
Seminarul VII
Tema: Aditivii alimentari (3ore)
Subiectele:
1. Caracteristica proprietatilor fizico-chimice si functionale a aditivilor alimentari:
coloranti,
conservanti,
antioxidanti,
gelifianti,
emulgatori,
aditivi de corectare a gustului alimentelor,
antispumanti,
stabilizatori ai structurii alimentelor.
2. Principiile de utilizare a aditivilor alimentari in tehnologiile de fabricare a produselor alimentare.
III. LUCRARI DE LABORATOR
Lucrarea de laborator nr.1
DETERMINAREA CANTITATII DE APA LEGATA IN PRODUSE VEGETALE
In fructe si legume continutul global de apa constituie 90-95%. In materia prima continutul apei este variat, in limitele de la 5% pana la 90%. Apa se afla in stare libera si legata.
Apa legata are un rol important, influentand activitatea apei, stabilitatea biochimica si microbiologica a produselor.
Scopul lucrarii: Determinarea apei legate si apei libere in produsele vegetale.
- Principiul metodei
Metoda se bazeaza pe procesele de osmoza ale tesutului vegetal in solutii hipertonice de zaharoza. In rezultatul difuziei apei libere din proba vegetala examinata, concentratia solutiei de zaharoza se reduce. Diferenta dintre concentratia solutiei dupa procesul de osmoza se determina prin metoda refractometrica. Apa legata se mentine in tesutul vegetal si poate fi identificata prin diferenta dintre apa totala si cea libera, care a trecut in solutie.
- Aparate si reactivi
Balanta tehnica; aparatul Cijov, pentru determinarea rapida a apei totale din proba; refractomeru; baloane conice de 100-200 cm3; baghete de sticla; hartie de filtru; exicator; produse vegetale: legume, fructe; solutie de zaharoza 25-30%.
3. Modul de lucru
3.1. Pregatirea probei pentru
analiza. Produsul initial se taie sub forma de felii cu
grosimea de 1-
3.2. Cu ajutorul refractometrului se determina concentratia initiala a zaharozei (C, %).
3.3. In doua baloane conice se introduc cate 25 cm3 solutie de zaharoza. Baloanele se cantaresc pana si dupa introducerea solutiei cu o precizie de 0,01 g., pentru a cunoaste cu precizie masa solutiei de zaharoza introduse.
3.4. In fiecare balon se introduc suplimentar cate 4-
3.5. Baloanele cu proba prealabil agitate se lasa in repaus 1, 5 ore. In acest timp apa libera a probei sub influenta presiunii osmotice trece in solutia de zaharoza. Are loc diluarea solutiei de zaharoza.
Determinarea apei totale in mostrele examinate se efectueaza prin uscarea probei cu ajutorul aparatului Cijov - metoda rapida (prezentata in anexa). Concentratia apei totale in proba se exprima prin Wt, %.
Dupa 1,5 ore continutul baloanelor se agita cu bagheta de sticla, se lasa in repaus 1-2 minute. Cu ajutorul refractometrului se determina concentratia solutiei de zaharoza.
Modul de calcul
Cantitatea apei libere in produsele vegetale se calculeaza din relatia:
![]()
X = 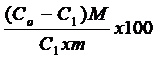 , (1)
, (1)
unde X este continutul apei libere in produs, %
Co - concentratia initiala a solutiei de zaharoza, %
C1 - concentratia solutiei de zaharoza dupa tratarea probei, %;
M - masa solutiei de zaharoza utilizata, g
m - masa probei produsului, g
Cantitatea apei legate se calculeaza prin relatia:
![]() Wl = W t - X , (2)
Wl = W t - X , (2)
unde Wl este continutul apei legate in produs,
Wt - continutul apei totale, %
X - continutul apei libere,%
Se efectueaza cate 3 determinari in ambele probe. Rezultatul final reprezinta media aritmetica a datelor obtinute.
Interpretarea rezultatelor
In baza datelor experimentale se fac concluzii referitor la cantitatea de apa libera si legata in produsele vegetale.
Lucrarea de laborator nr. 2
DETERMINAREA 5-OXIMETILFURFUROLULUI IN PRODUSELE ALIMENTARE TRATATE TERMIC
Tratarea termica a produselor alimentare in special de origine vegetala, provoaca diferite reactii chimice( caramelizarea mono- si dizaharidelor, interactiunea aminoacizilor si proteinelor cu zaharurile reducatoare etc. Ca rezultat se formeaza substante de culoare bruna, melanoidinele, substante de caramelizare, compusi polimerizati.
5- oximetilfurfurolul (5-O.M.F.) se formeaza in procesele de caramelizare prin mecanismul reactiei Maillard, acumulandu-se in produsele tratate termic. Concentratia O.M.F. in produse (sucuri concentrate, lapte concentrat, alimente pentru copii, mierea etc.) reflecta nivelul de tratare termica, modificarea culorii si valoarea nutritiva a alimentelor. De exemplu, daca concentratia O.M.F. nu depaseste limitele 1,0 -5,0 mg/kg, calitatea produselor se apreciaza pozitiv.
Scopul lucrarii: Determinarea continutului de O.M.F. in alimente. Aprecierea nivelului de modificare a calitatii produselor examinate.
- Principiul metodei
Determinarea O.M.F. se bazeaza pe metoda lui Winkder. O.M.F. in prezenta acidului butiric si a p-toluidinei formeaza o substanta rosie. Prin metoda calorimetrica , la lungimea de unda 540 nm se determina densitatea optica a complexului colorat, care este folosita la calcularea concentratiei O.M.F.
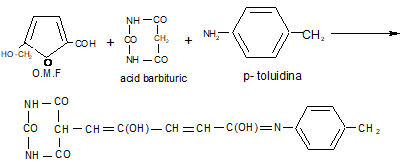 substanta rosie
substanta rosie
- Reactii si materiale
Produs pentru cercetare (suc concentrat, pasta) - 50g.; acid barbituric, concentratia - 5 mg/cm3; p - toluidina; concentratia - 0,1 g/cm3; solutia Karrer (K4Fe(CN)4 ; concentratia -0,15 g/cm; solutia Zn(CH3COO)2 sau ZnSO4 ; refractometru ; fotocolorimetru,pipete de 1 cm3, 2 cm3 ; 5cm3; 10 cm3; 50 cm3; 50 cm3, eprubete cu dop, baloane conice de 100 cm3, palnie de sticla.
3. Modul de lucru
In produsul initial se determina concentratia substantelor uscate prin metoda refractometrica.
. Intr-un pahar de 50 cm3 se cantaresc 10-15 g de produs cu o precizie de 0,2 g. Proba cantarita se dizolva cu 20-30 cm3 de apa distilata si se trece cantitativ intr-un balon cotat de 100 cm3 (volumul solutiei in balon nu trebuie sa depaseasca 80 cm3).
. Pentru limpezirea solutiei in balon cu proba se introduc:
- 1,5 cm3 solutie Karrer;
- 1,5 cm3 solutie de ZnSO4 sau Zn(CH3COO)2 .
Amestecul se aduce la cota cu apa distilata. Substantele colorate din proba formeaza un precipitat (polifenoli, proteine).
Dupa 5-10 minute, solutia din balonul cotat se filtreaza prin filtru de hartie. Filtratul trebuie analizat fotocolorimetric.
Fotocolorimetria In doua eprubete (1 si 2) se introduc cate 3,0 cm3 de filtrat si cate 5,0 cm3 solutie de p-toluidina. Solutiile se agita bine. Apoi in eprubeta 1se introduce 1,0 cm3 apa distilata ( proba martor), iar in eprubeta 2 se introduce 1,0 cm3 de solutie de acid barbituric. Eprubetele se agita (tabelul 1).
Tabelul 1
Pregatirea probelor pentru fotocolorimetrie
|
Nr. ord. |
Denumirea componentelor |
Eprubeta 1 |
Eprubeta 2 |
|
Proba martor, cm3 |
Proba pentru cercetare, cm3 |
||
|
|
Produsul diluat si filtrat |
|
|
|
|
Solutia p - toluidina |
|
|
|
|
Solutia acid barbituric |
|
|
|
|
Apa distilata |
|
|
Proba martor din eprubeta 1 si proba pentru cercetare (eprubeta 2) se introduc in 2 cuvete de 10mm. Se fotocolorimetreaza la lungimea de unda 540 ± 10 nm.
Atentie! Determinarea densitatii optice a solutiei de cercetare se efectueaza timp de 2-3 min,, inregistrand valoarea maxima a densitatii optice. Dupa 3-4 minute complexul rosu al O.M.F. se descompune si densitatea optica scade brusc. Pentru calcularea concentratiei O.M.F. trebuie de luat valoarea maxima a densitatii optice.
4. Modul de calcul
Concentratia O.M.F. in produs se calculeaza cu ajutorul relatiei (1):
O.M.F. = 0,066 ![]() x 1000 (1)
x 1000 (1)
unde O.M.F. este concentratia 5-oximetilfurfurolului in produs, mg/dm3;
0,066 - cantitatea de O.M.F. mg/ml din curba de etalon;
D - densitatea optica maximala a probei de cercetat;
Vo - volumul initial al produsului dizolvat ( Vo 100 cm3);
V1 - volumul de solutie al produsului folosit pentru fotocolorimetrie, cm3;
G - masa probei a produsului, g
In caz daca proba produsului nu a fost dizolvata cu apa distilata, concentratia O.M.F. in produs se calculeaza in baza relatiei (2):
O.M.F.
0,666![]() x 1000 (2)
x 1000 (2)
5. Interpretarea rezultatelor
In baza datelor experimentale se fac concluzii referitor la influenta tratamentului termic asupra continutului de 5-oximetilfurfurol in produsele alimentare.
Lucrarea de laborator nr. 3
DETERMINAREA COLORANTILOR NATURALI SI SINTETICI IN PRODUSELE ALIMENTARE
Culoarea alimentelor reprezinta o caracteristica importanta din punct de vedere tehnologic, comercial si nutritiv, jucand un rol important in aprecierea calitatii produselor alimentare. Ea depinde de continutul pigmentilor (clorofila, caroteni, antociane, polifenoli), continutul de coloranti naturali si sintetici.
In industria alimentara sunt utilizati atat coloranti naturali, cat si sintetici.
Utilizarea colorantilor sintetici in industria alimentara este reglementata de normele sanitare ale organizatiei Codex Alimentarius. Ei nu trebuie sa fie toxici, si sa nu constituie un risc pentru sanatate.
Scopul lucrarii: Identificarea colorantilor naturali si sintetici in produsele alimentare
Principiul metodei:
Metoda se bazeaza pe proprietatile proteinelor a fibrelor de lana de a absorbi colorantii sintetici, pe cand cei naturali nu sunt absorbiti.
2. Materiale si reactive:
o produse alimentare ( sucuri, bauturi alte produse colorate);
o acid clorhidric (HCl, d20 = 1,19, diluat 1: 9 v/v
o solutie de K2SO4, 10%;
o solutie de NaOH, 5%;
o solutie de NH4OH, 5%;
o fibre de lana special preparate pentru analiza
Degresarea fibrelor de lana
Fibrele de lana naturala se degreseaza cu eter (temperatura de 40 -60 o C) in aparatul Soxlet . Trebuie de efectuat 25-30 de sifonari. Lana se usuca, apoi timp de cateva minute se trateaza termic in solutie de NaON. Dupa aceea lana se spala atent cu apa si o uscam din nou la aer. Nu se recomanda de atins cu mana fibrele de lana.
3. Modul de lucru:
Pregatirea probei pentru analiza
3.1. Pentru analiza se iau 30-40 cm3 de produs si se determina valoarea pH la ionometrul In caz daca produsul este concentrat, atunci pentru analiza se iau numai 10-15 cm3 si se dilueaza cu apa distilata pana la volumul de 30-40 cm3.
3.2. Daca valoarea pH -ul solutiei a fost mai mic decat 6-7, proba se neutralizeaza cu amoniac (5%) pana la valoarea pH-ului 7,0. Neutralizarea se efectueaza in felul urmator. In solutie se introduc electrozii ionomerului . Cu ajutorul unei biurete se adauga solutia NH4OH pana cand pH-ul atinge valoarea 6,7-7,0. Solutia se agita permanent.
3.3. Dupa neutralizare in solutie se introduc 5 ml de K2SO4 . Paharul cu solutie se incalzeste pana la fierbere in baia de apa. In solutie se introduce o portiune de fibre de lana degresate in prealabil. Se lasa in repaus 5 minute.
3.4. Peste 5 minute fibrele se extrag din solutie si se spala bine cu apa rece. . Se analizeaza culoarea fibrelor. Prezenta colorantilor sintetici este indicata prin colorarea lanii.
3.5.Solutia din care au fost extrase fibrele de lana se aciduleaza cu 3-4 picaturi de HCl, pana la pH-ul 3,0-5,0. In solutie se introduce alta portiune de fibre. Se lasa in repaus 10 minute.
3.6. Dupa 10 minute, lana se extrage, se spala si se examineaza culoarea ei. Se fac concluzii asupra colorarii lanii in mediul acid.
Prezenta colorantilor sintetici in produsele alimentare este indicata de colorarea lanii. Colorantii bazici se fixeaza mai bine pe fibrele de lana in mediu neutru sau slab alcalin. Colorantii acizi se fixeaza in medii acide, insa pot fi fixati slab si in medii neutre.
Daca colorantii sunt naturali, atunci lana ramane necolorata.
4.Interpretarea rezultatelor
In baza datelor experimentale se fac concluzii referitor la natura colorantilor.
Lucrarea de laborator nr. 4
DETERMINAREA GRADULUI DE ESTERIFICARE A SUBSTANTELOR PECTICE
Substantele pectice sunt heteropoliglucidele polimerice alcatuite din resturile moleculelor a acidului D- galacturonic: unite intre ele cu legaturi 1,4-glicozidice:
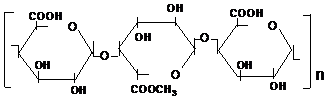
In macromolecula pectinei numarul gruparilor carboxilice
(-COOH) si a celor carboxilice metoxiate (-COOOCH3) este variabila. In functie de continutul gruparilor -COOH si
-COOOCH3 pectinele se impart in doua grupe:
pectina slab esterificata (metoxilata) - continutul gruparilor carboxilice (-COOH) este mai mare de 44% din numarul total de grupari carboxil si (-COOOCH3).
pectina puternic esterificata, contine mai mult de 44% de grupari metoxilate (-COOOCH3).din numarul total al gruparilor carboxil.
Raportul dintre continutul gruparilor carboxilice si carboxilice metoxilate (-COOH /-COOOCH3) determina proprietatile fizico-chimice ale pectinei: capacitatea de gelificare, absorbtia metalelor grele etc.
Scopul lucrarii: determinarea gradului de esterificare, metoxilare a substantelor pectice
Principiul metodei:
Gradul de esterificare a pectinei (%) se stabileste prin raportul volumului de NaOH, care se utilizeaza pentru determinarea gruparilor -COOH si -COOCH3. Determinarea gruparilor -COOH se efectueaza prin titrarea solutiei de pectina cu NaOH in prezenta indicatorului Hinton.
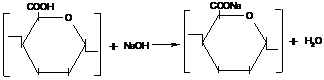
Gruparile -COOH se determina in primul rand -COOH prin procesul de saponificare a pectine:
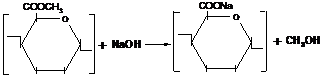
Numarul gruparilor -COONa, care s-au format in procesul de saponificare se determina prin a doua titrare a solutiei de pectina cu NaOH.
Materiale si reactivi
Vase conice Erhenmezer de 300 cm3 -2; baghete de sticla -2; biureta cu volum de 50 cm3-2, pipeta gradata 100 cm3 -1; pahar Berzelius de 100 cm3, hidroxid de sodiu (NaOH), 0,1 mol/dm3; acid clorhidric (HCl), 0,1 mol/dm3, indicator Hinton, pectina praf rafinata, alcool etilic 96%.
Modul de lucru
Determinarea gruparilor carboxilice in pectina
La balanta analitica se cantaresc doua probe de pectina rafinata a cate 0,3 . 0,5 g. Probele se trec cantitativ in vase conice de 300 cm3. Pentru a preveni formarea granulelor de pectina, proba se umecteaza cu cateva picaturi de alcool etilic de 96%.
In fiecare vas cu proba de pectina se adauga cate 100 cm3 apa distilata. Continutul se agita si se lasa in repaus 30 minute.
Dupa repaus vasele se incalzesc pana la temperatura de 40-60 o C si agitam solutia pana la dizolvarea completa de pectine.
In solutie se introduc cate 6 picaturi de indicator Hinton. Solutiile de pectina se titreaza cu NaOH (0,1 mol/l) pana la aparitia culorii roze, care este stabila cel putin 30 secunde.
Continutul gruparilor carboxilice in moleculele pectinei se calculeaza din relatia:
Kc = ![]() x 0,45 (1)
x 0,45 (1)
unde Kc este cantitatea gruparilor carboxilice, %;
V1 - volumul solutiei NaOH folosite pentru titrare, cm3;
G - masa probei de pectina luata pentru analiza, g;
0,45 - cantitatea de grupari -COOH (1,0 cm3 de NaOH corespunde 0,0045 g de grupari -COOH a pectinei prin titrare ).
Determinarea gruparilor carboxilice metoxilate
In solutia de pectina care a fost utilizata pentru determinarea gruparilor carboxilice libere, se introduc cate 50 ml NaOH 0,1 mol/l. casele conice se astupa cu dopuri. Mostrele se lasa in repaus 60 minute la temperatura camerei, pentru sapunificarea gruparilor carboxilice metoxilate.
Dupa aceea in solutia de pectina se adauga din biureta cate 50 ml de HCl 0,1 mol/l. Solutiile se agita. Apoi titram cu NaOH 0,1 mol/l pentru a neutraliza excesul de HCl.
Volumul de solutie NaOH, care a fost utilizat la a doua titrare (V2), corespunde cantitatii gruparilor esterificate (Ke) in proba analizata de pectina si se calculeaza astfel:
Ke = ![]() x0,45
x0,45
unde Ke - continutul gruparilor esterificate sau metoxilate, %;
V2 - volumul de solutie NaOH 0,1 mol/l utilizat pentru a doua titrare, ml ;
G - masa probei de pectina, g.
Continutul total al gruparilor carboxilice libere si esterificate in pectina cercetata se determina cu ajutorul formulei :
Kt = Kc + Ke (3)
unde Kt este continutul total al gruparilor carboxilice, %.
Gradul de metoxilare al pectinei se calculeaza astfel:
Me =![]() x 100
x 100![]() (4)
(4)
unde Me - gradul de metoxilare al pectinei, %
Gradul de
esterificare al pectinei se stabileste din relatia : ![]()
E=![]()
![]() (5)
(5)
unde E - gradul de esterificare al pectine, %
V1 - volumul solutiei de NaOH 0,1 mol/l utilizat la prima titrare,ml;
V2 - volumul solutiei de NaOH 0,1 mol/l utilizat la a doua titrare,ml;
4.Interpretarea rezultatelor
Din datele obtinute se determina media aritmetica a gradului de esterificare al pectinei. Se fac concluzii referitor la gradul de esterificare a substantelor pectice.
Lucrarea de laborator nr. 5
METODE DE IDENTIFICARE A PROTEINELOR
Proteinele sunt biomacromolecule care prin structura si proprietatile lor constituie insasi suportul material al vietii. In organismele vii ele se caracterizeaza printr-o mare variabilitate, fiind specifice in functie de organ si de specie. La baza formarii proteinelor stau cei 20-30 aminoacizi proteinogeni, uniti intre ei sub forma de lanturi polipeptidice. Proteinele sunt substante solide, amorfe, rar cristaline.
Solubilitatea in apa depinde de masa lor moleculara si de prezenta la suprafata a unor grupari hidrofile (-COOH; -NH2; -OH).
Scopul lucrarii: insusirea metodelor de identificare a proteinelor in compozitii alimentare.
Principiul metodei
Metoda de identificare a proteinelor se bazeaza in principiu pe doua tipuri de reactii: de culoare si de precipitare.
Identificarea proteinelor se bazeaza pe reactii tipice de precipitare, care pot fi reversibile si ireversibile.
Precipitarea reversibila: proteinele sufera o serie de modificari fizico-chimice, dar nu are loc distrugerea structurii moleculare. Cauza o constituie pierderea unei parti din apa de hidratare a proteinei. Are loc precipitarea, floculizarea sau coagularea. Se poate produce o rehidralizare prin adaugare de apa, proces care are loc la restructurizarea unor produse alimentare conservate prin uscare.
Precipitarea ireversibila este datorata denaturarii macromoleculelor . Consta in modificarea structurii spatiale, secundare si tertiare a proteinelor, care isi pierd proprietatile, trecand de la o configuratie ordinara a moleculelor proteice la o stare dezordonata. Masa moleculara nu se modifica. Agentii care determina denaturarea proteinelor pot fi de natura fizica (caldura), mecanica (agitarea), sau chimica (actiunea acizilor, bazelor, sarurilor).
Denaturarea proteinelor conduce si la inactivarea enzimelor si microorganismelor, stand la baza unor procedee de conservare a alimentelor.
Reactia de culoare. Prin reactii specifice proteinele interactioneaza cu ionii de cupru. Reactia de culoare este datorita prezentei sulfului; este specifica pentru proteine care contin tiaminoacizii si elibereaza prin incalzire in mediul puternic alcalin ionii de sulf. Acestia formeaza in prezenta acetatului de plumb sulfura de plumb de culoare neagra.
Materiale, aparate si reactivi
Balanta tehnica, pahar de sticla de 100 cm3; eprubete; pipete; baghete de sticla; mojar; clorura de potasiu KCl, 0,5 n; carbonat de sodiu NaHCO3, 100 ml, 0,5 n; KCl+0,25 g Na HCO3; hidroxid de sodiu NaOH, 0,5 n si 2n; sulfat de cupru, 0,1 %; acetat de plumb Pb(CH3 COO)2 1%; hidrohid de sodiu 20%; produse: carne, faina, suc natural.
Modul de lucru
Extractia proteinelor din produsele alimentare
din carne:
25 g carne slaba se spala cu apa rece pentru indepartarea urmelor de sange. Se marunteste fin. Tratam proba cu 100 cm3 solutie de 0,5 n KCl, care contine 0,25 g NaHCO3. Amestecam bine proba si dupa circa 30 minute o filtram prin tifon.
Prin tifon trece proteina solubila miozina, care se precipita prin diluarea extractului cu un volum de apa de 5-10 ori mai mare.
din produse vegetale:
Intr-un mojar se amesteca 5 g de faina cu 100 cm3 de solutie NaOH 0,5 n timp de 10 minute. Pentru analiza utilizam solutia obtinuta in urma decantarii si centrifugarii ( τ = 5 min,
n = 3000 rot / min).
Reactia biuretica
Se trateaza 5 ml dintr-o solutie proteica cu acelasi volum de NaOH 2n,. Apoi se titreaza cu solutie diluata de CuSO4 0,1%, pana la aparitia culorii violete. In cazul peptidelor, culoarea este roz-pal. Intensitatea culorii compusilor formati cu ionii de cupru este proportionala cu cantitatea proteinelor si deci poate fi folosita la dozarea proteinelor prin metode moderne (colorimetrice, spectofotocolorimetrice).
Reactia de culoare
Reactia de culoare este datorata prezentei sulfului. Intr-o eprubeta se introduc 5 cm3 solutie de acetat de plumb 1%. Apoi se introduce solutia de NaOH de 20% pana cand precipitatul de Pb(OH)2 se dizolva in excesul de hidroxid. Se adauga 4-5 ml extract de proteina. Proba o aducem pana la fierbere. Apare un precipitat brun.
4. Interpretarea rezultatelor
In baza datelor experimentale se fac concluzii referitor la natura si proprietatile proteinelor.
Lucrarea de laborator nr. 6
DETERMINAREA INDICELUI DE PEROXID AL LIPIDELOR
In procesul de oxidare al lipidelor apare o gama de compusi chimici ca: peroxizi, hidroperoxizi, aldehide, cetone etc. Ca urmare, in alimente (grasimi) apare un miros si gust neplacut, caracteristic gustului de "ranced".
In procesele de oxidare a lipidelor in faza initiala apar peroxizii, care apoi se transforma in hidroperoxizi, epoxizi s.a. Continutul de peroxizi si hidroperoxizi caracterizeaza prospetimea lipidelor. Pentru aprecierea nivelului de oxidare a lipidelor se determina indicele de peroxid, care poate fi exprimat prin numarul de grame de iod molecular (I2) pus in libertate de catre peroxizii din 100 g de lipide, tratate cu solutie de iodura de potasiu(KI).
Scopul lucrarii: insusirea metodelor de evaluare a indicelui de peroxid al lipidelor.
Principiul metodei
Metoda se bazeaza pe proprietatile peroxizilor de a elibera iodul molecular din iodura de potasiu in mediul acid:
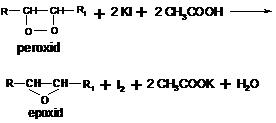
In prezenta hidroperoxizilor:
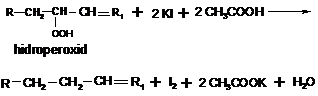
Iodul molecular eliberat prin reactia intre hidroperoxizii si KI este foarte activ si poate fi legat de catre legaturile duble ale acizilor grasi nesaturati din componenta gliceridelor, ce va conduce la o eroare la determinarea indicelui de peroxid. Pentru a bloca aceasta reactie, titrarea iodometrica se efectueaza in mediu de cloroform + acid glacial (2:1). Aciditatea ridicata a mediului de titrare blocheaza practic fixarea iodului molecular de catre legaturile duble ale acizilor grasi nesaturati.
Materiale si reactivi
Lipide : ulei vegetal; unt; iodura de potasiu (KI), solutie saturata; cloroform + acid acetic, (2:1); tiosulfat de sodiu
(Na2S 2O3),0,001n; solutie de amidon, 1,0 %; flacon iodometri, 100-200 cm3.
Modul de lucru
Intr-un flacon iodometric se cantaresc 1,0 . 2,0 g de grasime. In proba se adauga 15,0 cm3 amestec de cloroform + acid acetic glacial si 1,0 cm3 de solutie saturata de iodura de potasiu (KI).
3.2. Balonul se agita. Se mentine in repaus timp de 20 minute la intuneric. In acest timp are loc interactiunea peroxizilor cu KI si se elibereaza I2.
3.3. Dupa repaus in balon se introduc 50 cm3 de apa distilata si 1,0 cm3 de solutie de amidon 1,0 %.
Amestecul imediat se titreaza cu solutie de tiosulfat de sodiu (Na2 S2 O3), proba martor.
3.5. Concomitent in aceleasi conditii se prepara si proba martor (fara grasime). Se trateaza conform punctelor 3.1- 3.4.
Modul de calcul
Indicele de peroxid se stabileste in % conform formulei:
IP=![]()
![]() (1)
(1)
unde IP este indicele de peroxid al grasimii analizate, %;
V1 - volumul de Na2 S2 O3 0,001 n utilizat la titrarea probei de analizat, cm3;
0,0127 - titrul 0,001 n solutiei de Na2 S2 O3 in raport cu iodul molecular (I2) inmultit cu 100 %;
V2 - volumul de Na2 S2 O3 0,001 n utilizat la titrarea probei martor, cm3.
M- masa probei de grasime, g.
Interpretarea rezultatelor
In baza datelor experimentale se fac concluzii referitor la indicele de peroxid al lipidelor.
Anexa
Determinarea substantei uscate totale cu raze infrarosii in aparatul Cijov. Metoda rapida gravimetrica
- Principiul metodei
Deshidratarea produsului supus analizei are loc sub influenta razelor infrarosii cu lungimea de unda 700nm, care patrund usor in produs la adancimea de 23 mm. Apa ce se contine in proba este usor si rapid eliminata. Metoda este folosita la analiza fructelor, legumelor si radacinoaselor. Lucrarea de laborator nr. 6
Modul de lucru
In aparatul Cijov sursa de radiatii infrarosii sunt doua placi metalice masive care se incalzesc cu energie electrica. In aparat deshidratarea produselor omogenizate a legumelor, fructelor se executa in pachete de hartie la parametrul timp-temperatura 5 minute la 150-155 o C.
Pachetele de hartie se pregatesc in felul urmator:
din hartie de ziar se
taie foi cu dimensiunile 20x14 cm, se indoaie in doua, marginile din
partile deschise se indoaie cu 1,5cm. Dimensiunile pachetului gata
sunt 8,5 x
separat, din hartie de filtru se pregateste anexa-pachet. Se taie o foaie cu dimensiunile 25 x11 cm, care se indoaie in trei )8,3 x 11,0= in asa fel ca partea de jos sa fie doua straturi, iar partea de sus -un stat, care se introduce suplimentar in pachetul pregatirii din hartie de ziar.
Se pregatesc doua pachete ce se numeroteaza.
Pachetele pregatite se usuca in aparatul Cijov 3 minute la
temperatura 150-155 o C, se racesc in exicator 35 minute
si se cantaresc la balanta tehnica cu exacitatea de
Pachetele cantarite se introduc in aparatul Cijov si se usuca la temperatura si timpul indicat mai sus. Se racesc in exicator 3-5 minute, dupa ce se intaresc, greutatea se noteaza cu M2.
Continutul de apa (Xt, %) in fructe si legume uscate, materiale auxiliare se calculeaza dupa formula:
Xt =![]() (1)
(1)
unde Xt este continutul total de apa in legume, fructe;
M - greutatea pachetului uscat, g;
M1 - masa pachetului cu produs pana la uscare, g;
M2 - masa pachetului cu produs dupa uscare, g.
Ca rezultat se ia media aritmetica a doua determinari care nu difera intre ele cu cel mult 0,2%..
Bibliografia de baza
- C. Banu Tratat de chimia alimentara. Ed. AGIR, Bucuresti, 2002.
- A. Ghergi Biochimia si fiziologia legumelor si fructelor. Ed. Academia Romana, 2005.
- Norme si reguli sanitare privind aditivii alimentari.
WWW. Sanepid.md/docs/
- Chimia produselor alimentare. Ciclu de prelegeri. Partea I. P. Tatarov. U.T.M., 2007.
- Chimia produselor alimentare. Indrumar de laborator. Chisinau,f 1998.
- R. Segal Valoarea nutritiva a produselor agroalimentare. Ceres, Bucuresti, 1983.
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2024 - Toate drepturile rezervate -| |
|
|
|||
|
|||
Proiecte pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||








