
| Medicina | Medicina veterinara | Muzica | Psihologie | Retete | Sport |
Medicina
|
|
Qdidactic » sanatate & sport » medicina Aparatul respirator la nou-nascut (normal si patologic) |
Aparatul respirator la nou-nascut (normal si patologic)
Aparatul respirator la nou-nascut (normal si patologic)
Introducere
Majoritatea tulburarilor respiratorii care afecteaza nou-nascutul sunt rezultatul dificultatilor de adaptare de la viata intrauterina la cea extrauterina. Imaturitatea plamanului, incluzand productia inadecvata de surfactant pulmonar, este responsabila de cel mai mare procent de mortalitate la nou-nascutul prematur. Tulburarile care afecteaza in principal nou-nascutul la termen includ aspirarea de meconiu, a lichidului amniotic, persistenta hipertensiunii pulmonare si diverse anomalii congenitale. In general, infectiile perinatale afecteaza sistemul respirator si contribuie la cresterea semnificativa a morbiditatii si mortalitatii perinatale atat la nou-nascutul prematur cat si la nou-nascutul la termen.
Scopul terapiei pentru nou-nascutii cu disfunctii respiratorii este de a furniza suportul necesar pentru a asigura schimbul adecvat de gaze si transportul oxigenului necesar pentru supravietuire pe toata durata bolii.
Date de semiologie a tulburarilor respiratorii ale nou-nascutului Tahipneea
Este in general definita ca o frecventa respiratorie mai mare de 60 respiratii/minut. Sugarul cu o complianta pulmonara scazuta minimalizeaza efortul respirator prin respiratii rapide cu volume inspiratorii - expiratorii mici. De aceea tahipneea este prezenta de obicei la sugarii cu complianta pulmonara scazuta (ex. sindromul de detresa respiratorie), pe cand sugarii cu rezistenta crescuta a cailor respiratorii (ex. obstructia cailor respiratorii superioare) prezinta miscari respiratorii adanci, dar lente.
Dispneea
Este un sunet expirator produs de adductia corzilor vocale in timpul eliminarii aerului. Prin dispnee sugarul poate preveni colapsul alveolelor la sfarsitul expiratiei si reducand astfel suntarea pulmonara amelioreaza si oxigenarea.
Retractiile
Se refera la deplasarea spre interior a partilor moi ale peretelui toracic. Acestea sunt cel mai frecvent observate in regiunile intercostale si subcostale. Retractia sternala poate fi observata la nou-nascutul prematur datorita compliantei crescute a peretelui toracic. Retractiile sunt de obicei datorate compliantei pulmonare scazute sau a obstructiei cailor respiratorii.
Flaring-ul nazal
Este cresterea tremorului nazal in timpul inspiratiei. Deoarece rezistenta nazala si faringiana reprezinta 50 din rezistenta cailor aeriene la nou-nascut, efortul respiratiei este probabil scazut prin largirea foselor nazale.
Cianoza
Este coloratia albastra a tegumentelor si mucoaselor, care apare datorita unei cantitati crescute de hemoglobina desaturata in patul capilar.
In cianoza de tip central saturatia in oxigen a sangelui arterial este scazuta. Coloratia albastra a mucoaselor se observa la nivelul limbii si al gurii, completand coloratia pielii.
In cianoza de tip periferic pielea este cianotica, dar mucoasele sunt normal colorate.
Cianoza mainii si a piciorului (acrocianoza) este frecvent intalnita la nou-nascutul sanatos. Aceasta se datoreaza fluxului sanguin incetinit in patul capilar al acestor tesuturi, care au drept rezultat o extractie crescuta a oxigenului si astfel o concentratie crescuta a hemoglobinei desaturate.
Gradul cianozei este determinat de cantitatea totala de hemoglobina desaturata din sange. Pentru ca cianoza centrala sa fie vizibila cantitatea de hemoglobina desaturata din sangele arterial trebuie sa fie de cel putin 40-50g/l. De aceea, cianoza centrala va fi detectata la o saturatie arteriala relativ crescuta, cand concentratia hemoglobinei totale este crescuta. Din contra, cianoza centrala nu va putea fi detectata la sugarul anemic pana cand saturatia oxigenului in sangele arterial nu scade semnificativ.
Bolile respiratorii in neonatologie
Sindromul detresei respiratorii
Sindromul detresei respiratorii (SDR) este unul dintre cele mai frecvente boli respiratorii si este una din principalele cauze ale mortalitatii neonatale. In mod obisnuit pentru SDR se utilizeaza sinonime ca: boala membranelor hialine sau sindromul detresei respiratorii idiopatice.
Prematuritatea este cel mai important factor de risc pentru SDR. Incidenta sa este de 60 la 29 saptamani de gestatie si descreste odata cu cresterea varstei gestationale pana la zero dupa 39 saptamani.
Alti factori de risc pentru SDR includ: operatia cezariana fara travaliu, asfixia la nastere si diabetul matern.
SDR se dezvolta datorita imaturitatii pulmonare, a deficientei primare de surfactant. Surfactantul pulmonar este un amestec complex de fosfolipide si proteine produse de catre celulele alveolare de tip II; fosfolipidele formeaza un monostrat la interferenta gaz-lichid pe suprafata interna a alveolelor pulmonare. Datorita efectelor tensioactive ale monostratului are loc o scadere a tendintei alveolelor de a se colaba la sfarsitul expiratiei. Unul din principalele roluri ale proteinelor surfactantului este de a usura dispersia fosfolipidelor pe suprafata alveolara.
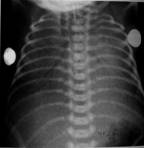
FIG.2 Opacifieri reticulo-granulare
difuze, bronhograma aerica si scaderea
volumului pulmonar la un
nou-nascut prematur cu SDR
Productia inadecvata de surfactant duce la colapsul alveolelor, microatelectazie si scaderea compliantei pulmonare. Efortul respirator este crescut si dezechilibrul dintre ventilatie si perfuzie duce la hipoxemie arteriala. Nou-nascutul cu SDR dezvolta detresa respiratorie imediat dupa nastere cu dispnee expiratorie, flaring nazal si retractia toracelui. Datele radiologice arata reducerea volumului pulmonar, bronhograma aeriana si opacitati fine granulare.(Fig. nr 2.)
Analizele uzuale ale gazelor sanguine descopera hipoxemie si hipercapnie.
Principalele obiective ale terapiei nou-nascutului cu SDR sunt suplimentarea cu oxigen, ventilatia asistata si suplimentarea surfactantului. La nou-nascutul cu respiratie spontana oxigenul este administrat de obicei prin suplimentarea cu oxigen a aerului din incubator sau prin nise directe de oxigen. Se considera ca presiunea pozitiva continua in caile respiratorii (CPAP), previne colapsul alveolar la sfarsitul expiratiei si astfel, scade nevoia suplimentarii oxigenului. Oxigenul este furnizat prin plasarea sondelor nazale sau prin intubatie nazofaringiana.
Ventilatia mecanica este utilizata la nou-nascutul cu SDR severa cand oxigenarea adecvata nu poate fi mentinuta prin suplimentarea oxigenului, cu sau fara CPAP. Este de asemenea necesara pentru nou-nascutul cu acidoza respiratorie progresiva (pH < 7,25.) Ventilatia mecanica poate fi realizata fie prin ventilatie conventionala, fie prin ventilatie cu frecventa crescuta.
Administrarea de surfactant se face nou-nascutului care necesita ventilatie mecanica pentru SDR. Surfactantul este administrat prin instilatii traheale direct pe tubul endotraheal. Acesta creste complianta pulmonara, creste oxigenarea prin scaderea raportului ventilatie/perfuzie si faciliteaza decuplarea de la ventilator. Posibilele complicatii ale administrarii de surfactant sunt hipotensiunea, hipoxia si bradicardia in timpul administrarii, blocajul tubului endotraheal sau al cailor respiratorii si hemoragia pulmonara. S-a demonstrat ca prin administrarea de surfactant mortalitatea prin SDR descreste cu 40-60 iar morbiditatea multisistemica se reduce, si scade incidenta bolilor cronice pulmonare.
Complicatiile SDR includ dezvoltarea unor fisuri aeriene pulmonare, persistenta canalului arterial, hemoragia intracraniana si, pe termen lung dezvoltarea bolilor cronice pulmonare.
Sindromul de aspiratie meconiala
Colorarea meconiala a lichidului amniotic survine in 10-15 din nasteri. Aproximativ jumatate din acesti nou-nascuti au meconiu in trahee dupa nastere. Aspirarea meconiului poate da complicatii respiratorii severe.
Eliminarea meconiului in uter este asociata de obicei cu asfixia intrauterina, postmaturitatea sau ambele. Hipoxia intrauterina are ca rezultat redistributia fluxului sanguin de la organele nevitale la inima, creier si glandele suprarenale. Aceasta redistributie este rezultatul reflexului de redirijare prin care se realizeaza transportul adecvat al oxigenului la organele vitale in timpul hipoxiei intrauterine. Hipoxia intestinala are ca rezultat unde peristaltice tranzitorii care pot explica scurgerea meconiului la fatul cu hipoxie intrauterina.
Colorarea meconiala a lichidului amniotic poate fi astfel un ,,marker'' al detresei fetale, mai ales cand aceasta este corelata cu tulburari ale frecventei cardiace fetale.
Incidenta contaminarii lichidului amniotic cu meconiu creste cu prelungirea sarcinii. Aproximativ1/3 din nou-nascutii la 42 saptamani de gestatie sau mai tarziu au meconiu in utero.
Asfixia intrauterina poate determina aparitia gasp-urilor sporind riscul aspiratiei meconiale. Hipoxia intrauterina prelungita poate determina hipertrofia fibrelor musculare ale arterelor pulmonare. Astfel creste riscul persistentei hipertensiunii pulmonare care este de obicei prezenta in sindromul de aspiratie severa si face mai dificila conduita terapeutica a acestor nou-nascuti.
Prezenta meconiului in caile respiratorii cele mai mici poate determina obstructia partiala sau completa a acestora. Obstructia completa determina atelectazie datorita absorbtiei gazului situat distal de obstructie. Obstructia partiala determina hiperinflatia portiunii distale pulmonare datorita unui efect de valva cu supapa unidirectionala.
Deoarece diametrul cailor respiratorii periferice este mai mare in timpul inspiratiei decat in timpul expiratiei acele cai aeriene partial obstruate cu meconiu in timpul inspirului pot deveni total obstruate in timpul expirului rezultand acumularea aerului distal de obstructie. Similar acumularea aerului si hiperinflatia pot determina pneumotorax sau alte defecte de etanseizare a aerului. In cele mai distale cai respiratorii, meconiul poate determina pneumonie chimica, impiedica actiunea surfactantului sau ambele, rezultand exsudatul alveolar, atelectazia si hipoxia arteriala ca o consecinta a dezechilibrului ventilatie/perfuzie.
Nou-nascutul care a aspirat meconiu prezinta de obicei semnele detresei respiratorii in sala de nastere. Diametrul antero-posterior al toracelui este de obicei crescut datorita hiperinflatiei plamanilor.
La auscultatia toracelui se aud raluri bronsice.
Examenele radiologice releva cresterea volumelor pulmonare cu zone opace de atelectazie si hiperinflatie focala.
Pentru a scadea riscul aspiratiei meconiale in timpul nasterii la termen este importanta aspirarea meconiului din gura si nazo-faringe.
Deoarece aspiratia meconiului poate avea loc si inainte de nastere aspirarea directa din trahee este eficienta mai ales daca se suspecteaza hipoxia intrauterina. Pentru nou-nascutul care dezvolta detresa respiratorie ar trebui instituita oxigenoterapia sustinuta cu suplimentarea rezervelor de oxigen deoarece hipoxemia predispune la hipertensiune pulmonara. Daca oxigenarea adecvata nu poate fi mentinuta prin concentratia crescuta a oxigenului in aerul inspirat trebuie instituita ventilatia mecanica. Administrarea de surfactant exogen pare sa scada severitatea sindromului de aspiratie meconiala.
Disfunctia respiratorie a nou-nascutului prin operatie cezariana selectiva
Este deja recunoscut faptul ca operatia cezariana selectiva, fara travaliu contribuie la cresterea riscului pentru disfunctii respiratorii. Acest risc este in relatie inversa cu varsta gestationala. In majoritatea cazurilor aceasta este o tulburare respiratorie tranzitorie si benigna. Totusi unii nou-nascuti dezvolta disfunctii respiratorii severe care au fost asociate cu morbiditate si chiar mortalitate crescuta.
Patogeneza tulburarilor pare sa fie heterogena si pot fi implicati 3 factori diferiti:
clearance inadecvat al lichidului pulmonar avand drept consecinta tahipneea tranzitorie,
deficitul de surfactant rezultand SDR si
persistenta hipertensiunii pulmonare.
Clearance-ul inadecvat al lichidului pulmonar dupa operatia cezariana fara travaliu are drept consecinta de obicei detresa tranzitorie a nou-nascutului. S-a presupus ca aceasta se datoreaza lipsei cresterii nivelului de catecolamine, crestere importanta pentru un clearance normal al lichidului pulmonar. Aceasta crestere se produce in mod normal in timpul travaliului, dar ea este mult mai mica in operatia cezariana selectiva. Ca urmare a clearance-ului insuficient al lichidului pulmonar asociat cu operatia cezariana lipseste compresiunea toracelui care se produce in mod normal in timpul trecerii prin filiera pelvi-genitala. Din aceste motive, felul cum se deruleaza nasterea este important pentru a anticipa probabilitatea ca un nou-nascut sa dezvolte o disfunctie respiratorie.
Daca operatia cezariana este realizata inainte ca sistemul surfactant pulmonar sa atinga maturizarea completa nou-nascutul dezvolta SDR.
Nou-nascutul prin operatie cezariana selectiva pare a fi supus unui risc crescut de dezvoltare a hipertensiunii pulmonare. S-a demonstrat prin ecocardiografie ca acesti nou-nascuti au o scadere mai lenta a presiunii in arterele pulmonare decat cei nascuti fiziologic.
Pneumonia neonatala
Debutul rapid al pneumoniei bacteriene este cel mai frecvent cauzat de aspirarea lichidului amniotic contaminat dupa ruperea prematura a membranelor sau de aspirarea secretiilor vaginale intranatal, la trecerea prin filiera pelvi-genitala.
Cei mai frecventi agenti patogeni ai pneumoniei nou-nascutului sunt: Streptococii de grupB, Escherichia coli si Enterococii. Hemophilus influenzae, Streptococcus viridans si anaerobii determina mai rar boala. Listeria monocytogenes si Treponema pallidum pot determina pneumonie la fat prin pasaj transplacentar.
Factorii predispozanti ai pneumoniei nou-nascutului sunt nasterea prematura, ruptura membranelor inainte de debutul travaliului (ruptura membranelor cu 24 de ore sau mai mult inainte de nastere) si inflamatia corio-amniotica materna.
Nou-nascutul cu pneumonie congenitala dezvolta sindromul detresei respiratorii intr-un interval mai scurt de la nastere. Aspectul radiologic este nespecific si aceasta stare poate fi greu diferentiata de SDR. Antibioticele de electie pentru pneumonia nou-nascutului sunt Ampicilina si unele Aminoglicozide.
Pneumonia cu debut tardiv sau nosocomial apare de obicei la nou-nascutii care necesita suport respirator prelungit. Acesti nou-nascuti sunt de obicei intubati ceea ce ofera calea de acces a microorganismelor catre plamani. Microorganismele incriminate sunt: Staphilococus aureus, Staphilococus epidermidis, Pseudomonas aeruginosa si Escherichia coli.
Prematurii prezinta un risc particular pentru infectiile nosocomiale deoarece ei au un raspuns imun scazut. Cei mai multi prematuri prezinta riscul de a face pneumonie cu Candida albicans.
Displazia bronhopulmonara
Displazia bronhopulmonara este forma majora a bolilor cronice pulmonare in neonatologie. Apare frecvent la prematurii cu suport ventilator prelungit pentru tratamentul SDR. Incidenta este estimata la 40-70 din prematurii sub 1000g. Aceasta boala este de asemenea intalnita la nou-nascutii la termen care necesita ventilatie asistata prelungita din cauza afectiunilor pulmonare severe ca: sindromul de aspiratie, persistenta hipertensiunii pulmonare, hernia diafragmatica sau boli congenitale cardio-pulmonare.
Cei mai importanti factori in patogenia displaziei bronhopulmonare sunt toxicitatea oxigenului, ventilatia mecanica si imaturitatea plamanului. Expunerea prelungita la concentratii de oxigen > de 60 este daunatoare pentru plamani. Principalul mecanism al toxicitatii oxigenului este formarea de radicali liberi de oxigen care determina leziuni celulare prin peroxidarea membranelor lipidice celulare, prin inactivarea enzimelor sulfhidril, prin dereglari ale acizilor nucleici. Plamanul normal este echipat cu enzime antioxidante pentru protectia fata de injuriile determinate de radicalii liberi de oxigen. Aceste enzime protectoare urmaresc modelul de maturatie al sistemului surfactant si activitatea lor poate fi slab dezvoltata la nou-nascutul prematur.
Ventilatia mecanica cu presiune de inflatie crescuta poate cauza intinderea excesiva a plamanilor rezultand distensia sau ruptura cailor respiratorii mici si a alveolelor. Astfel poate apare emfizemul interstitial sau evacuarea extrapulmonara a aerului, stari precursoare ale displaziei bronhopulmonare.
Alti factori ce pot contribui la dezvoltarea displaziei bronhopulmonare cuprind infectiile nosocomiale, edemul pulmonar cauzat de persistenta permeabilitatii ductului arterial si nutritia inadecvata, inclusiv deficitul de vitamina A.
Datele clinice din displazia bronhopulmonara includ toracele ,,in butoi'' (emfizematos), tahipnee, retractii si wheezing-ul expirator. Testarea functiei pulmonare releva cresterea rezistentei cailor respiratorii si scaderea compliantei pulmonare dinamice, care sporeste efortul respiratiei. Ventilatia este distribuita inegal, rezultand hipoxemie arteriala datorata perturbarii raportului ventilatie/perfuzie. Apare hipercapnia. Radiografia toracica tipica arata cresterea volumelor pulmonare cu arii de atelectazie alternand cu arii de hiperinflatie, ce pot deveni chistice
Apneea de prematuritate
Apneea este definita ca o incetare a respiratiei pentru mai mult de 20 de secunde sau orice pauza respiratorie cu durata mai scurta care este asociata cu cianoza, bradicardie sau ambele. Apneea survine frecvent la nou-nascutul prematur. Este cauzata de obicei de o tulburare tranzitorie a controlului respirator(apneea de prematuritate) sau mai rar de o stare grava ca: septicemia, hipoglicemia, hemoragia intracraniana, crizele comitiale sau ingestia unor medicamente de catre mama. Deci apneea de prematuritate este un diagnostic de excludere. Apneea nou-nascutului la termen nu trebuie considerata niciodata fiziologica. Ea necesita o evaluare completa pentru a determina cauza sa.
Incidenta apneei de prematuritate este in relatie indirecta cu varsta gestationala. Apneea de prematuritate pote fi impartita in 3 tipuri : centrala, obstructiva , mixta.
a. Apneea centrala- este determinata de imaturitatea centrului de control respirator bulbar. Acesti nou-nascuti au un raspuns scazut la dioxidul de carbon, care este un etalon al reglarii respiratorii.
|
b. Apneea obstructiva survine datorita hipotoniei muschilor faringieni, a pozitiei incorecte a capului fatului (in special pozitia de flexie) sau datorita unor secretii in caile aeriene superioare. De asemenea diafragmul nou-nascutului prematur se poate contracta inainte de cresterea tonusului muschilor cailor aeriene superioare, contractie care survine in mod normal in timpul inspiratiei si astfel predispune nou-nascutul la apnee obstructiva. In apneea obstructiva nou-nascutul continua sa prezinte miscari ale peretelui toracic. De aceea ea nu este detectata prin monitorizare cardio-respiratorie uzuala pana cand cianoza sau bradicardia nu s-au instalat.
Ar trebui instituita monitorizarea continua a respiratiei si a frecventei cardiace la toti prematurii. Daca apneea survine, este important sa se identifice si sa se trateze orice cauza care determina aparitia sa.
Apneea usoara raspunde de obicei la stimulare tactila.
Apneea mai severa poate necesita ventilatie mecanica cu balon pe masca. Daca episoadele de apnee survin frecvent si sunt prelungite ar trebui introdus tratament suplimentar pentru a preveni aparitia leziunilor hipoxice la nou-nascut.
Metilxantinele, teofilinele si cafeinele scad numarul si severitatea apneilor centrale prin cresterea sensibilitatii centrului respirator bulbar la dioxid de carbon. Aplicarea presiunii continue pozitive in caile respiratorii reduce numarul crizelor de apnee, in special a celor de apnee obstructiva, mentinand deschis canalul faringian.
Episoadele severe de apnee nu raspund la aceste modalitati terapeutice si necesita intubatie endotraheala si ventilatie mecanica. Frecventa si severitatea crizelor de apnee descreste odata cu cresterea varstei gestationale si ele sunt rare dupa 37 de saptamani de gestatie. Se recomanda ca acei prematuri care au un istoric de apnee sa fie externati doar atunci cand nu mai prezinta crize de cel putin o saptamana, in absenta terapiei cu metilxantine.
Hernia diafragmatica congenitala
Hernia diafragmatica congenitala reprezinta o herniere a continutului abdominal in torace printr-un defect al diafragmului. Hernia diafragmatica congenitala survine cu o frecventa de 1/2500 si este asociata cu o rata cosiderabila a morbiditatii si a mortalitatii neonatale.
Defectul diafragmului survine datorita perturbarii inchiderii canalului pleuroperitoneal in timpul saptamanii a 8-a de gestatie.
Defectul este situat mai frecvent pe partea stanga la nivelul trigonului lombocostal postero-lateral (hernia lui Bochdalek). Daca hernia survine mai devreme in viata fetala ea este asociata cu diferite grade de hipoplazie pulmonara.
Plamanul de partea afectata este mic, la acest nivel exista o marcata reducere a numarului de generatii bronsice si numarul vaselor de tip arterial este redus proportional. In plus, exista o crestere a musculaturii mediei arterelor pulmonare la nivel acinar, crescand astfel rezistenta in circulatia pulmonara. Nou-nascutul cu aceste modificari prezinta un risc considerabil pentru hipertensiune pulmonara cu sunt stanga-dreapta prin foramen ovale si canalul arterial. Hipoplazie pulmonara intr-un grad mai mic exista si de partea contralaterala.
Nou-nascutul cu hernie diafragmatica congenitala si hipoplazie pulmonara prezinta de obicei detresa respiratorie la scurt timp dupa nastere. Sonoritatea pulmonara este absenta de partea afectata, toracele este emfizematos si abdomenul este scafoid. Zgomotele cardiace sunt de obicei deplasate .Acesti copii au grade diferite hipoxemie arteriala, hipercapnie si acidoza.
Nou-nascutii care au hipoplazie pulmonara minima sau absenta pot fi asimptomatici la nastere, dar dezvolta mai tarziu detresa respiratorie, cand are loc acumularea progresiva, fiziologica a aerului in stomac si intestin si se produce compresiune asupra organelor intratoracice.
Diagnosticul se pune pe radiografia toracica dupa punerea unui tub de alimentatie in stomac. Ansele intestinale pline cu aer si stomacul pot fi vazute in torace. Inima este deplasata spre partea contralaterala si abdomenul este lipsit de gaze (excavat).
Inchiderea chirurgicala a defectului diafragmului este tratamentul definitiv. Corectarea acidozei si mentinerea unei perfuzii adecvate sunt obiective importante inainte de interventia chirurgicala.
Prognosticul nou-nascutului cu hernie diafragmatica congenitala este strans legat de gradul hipoplaziei pulmonare.
Principii si mijloace terapeutice in insuficienta respiratorie neonatala
Ventilatia asistata la nou-nascut
Oxigenoterapia de suplimentare
Cea mai simpla metoda de a creste continutul in oxigen al sangelui este de a creste fractia de oxigen inspirat ( FiO2) in timp ce utilizarea oxigenului suplimentar este cea mai comuna metoda in procesul de intrerupere a ventilatiei mecanice sau in asociere cu presiunea continua pozitiva in caile aeriene. Oxigenoterapia este deseori suficienta la prematurii peste 30 de saptamani, cu SDR, la toti nou-nascutii cu boala respiratorie minima si majoritatea celor cu tahipnee tranzitorie neonatala. Aceasta metoda poate fi folosita si la nou-nascutii la termen care prezinta SDR si la cei cu sindrom de aspiratie meconiala. Oxigenul cald si umidificat eliberat intr-o boxa de plexiglas (izoleta) plasata la extremitatea cefalica va realiza un mediu imbogatit cu oxigen. Crescand FiO2 se va scadea frecventa crizelor de apnee la nou-nascutul prematur.
Presiunea continua pozitiva in caile aeriene (CPAP)
Prin CPAP se mentine o presiune pozitiva de distensie in caile respiratorii, aplicata la o valoare mai mica de 8 cm. H2O, in timpul respiratiei spontane. De cand CPAP a fost inventata in 1971 de catre Gregory si col. ea a devenit cheia terapiei respiratorii in asistenta nou-nascutului. Importanta fiziologica specifica a acestei metode nu este pe deplin inteleasa, totusi o parte din eficienta sa este datorata directei ameliorari a functiei pulmonare printr-o actiune a mai multor mecanisme. (Tabel 2)
Principalele indicatii pentru CPAP:
SDR la nou nascutii peste 1500 g. (1500-2500 g.) (surfactant diminuat si capacitate reziduala pulmonara scazuta);
Lichid pulmonar neresorbit (tahipneea tranzitorie a nou-nascutului post operatie cezariana);
Respiratia neregulata (apneea de prematuritate/ apneea recurenta);
In cursul "indepartarii" nou-nascutului de la ventilator si dupa detubare;
In anumite obstructii ale cailor respiratorii superioare (ex. sindromul Pierre-Robin);
Cai respiratorii instabile ( traheomalacia, bronhomalacia, stridor laringian congenital).
Dupa detubare este preferabil CPAP nazo-faringian, varful canulei nazale fiind trecut dupa orificiile coanale posterioare, in epifaringe.
Datele recente arata ca utilizarea precoce a CPAP duce nu numai la imbunatatirea functiei pulmonare si reglarea respiratiei la prematurul suferind de SDR, dar scade si necesitatea utilizarii ventilatiei mecanice.
Setarile CPAP:
- Presiune: 5 - 7 cm. H2O
- Flux: 5 - 10 l/min.
- FiO2 - cel la care era copilul inaintea administrarii CPAP.
Aceste setari se modifica in functie de valorile gazelor sanguine, a caror monitorizare in dinamica este necesara.
Se folosesc sonde nazale sau un tub nazo-faringian. Sondele nazale au rezistenta minima si de aceea sunt preferate. CPAP nazal poate fi aplicata in ambele narine sau, printr-un tub, intr-o singura nara (tehnica preferabila). Se utilizeaza un tub de 3 mm. introdus 1 cm. intr-o nara si adaptat la ventilatorul mecanic ceea ce permite un bun control al presiunii, amestecului de gaze, fluxului si umidificarii aerului administrat. Deoarece un tub endotraheal are o rezistenta foarte mare CPAP administrata prin tub endotraheal ar trebui utilizata doar pe o perioada scurta de timp. Cu toate ca utilizarea CPAP este relativ benigna au fost observate unele complicatii sau efecte secundare.
Complicatiile si efectele secundare ale CPAP:
CPAP excesiva
creste spatiul mort pulmonar
impiedica intoarcerea venoasa
creste retentia de dioxid de carbon
creste presiunea intracraniana
creste efortul respirator
CPAP joasa
determina la un volum pulmonar inadecvat
determina retentie de dioxid de carbon
Complicatii generale
pneumotorax (<5%), survine mai frecvent in primele ore de viata-poate duce la producerea de hemoragie cerebrala.
aerofagia- determina distensie gastrica-in administrarea CPAP intotdeauna se introduce un tub nazo-gastric care se lasa in situ.
eroziunea sau necroza septului nazal.
In perioada acuta a afectiunii respiratorii se suspenda alimentatia enterala din cauza riscului de aspiratie ("cale falsa").
La nou nascutii mai mici de 1500 g. in timpul CPAP poate aparea colapsul brusc cu riscul producerii hemoragiei cerebrale si necesitatea ventilatiei mecanice, de aceea la acesti nou-nascuti este indicata ventilatia mecanica din start.
Daca tratamentul cu CPAP nu ajuta la mentinerea oxigenarii si ventilatiei la valori acceptabile trebuie initiata ventilatia mecanica (Tabel 5).
Definirea esecului CPAP:
q PaO2 < 50 mmHg ( 6,7 kPa ) cu FiO2=80-100%
q PaCO2> 65 mmHg ( 8,7 kPa )
q acidoza dificil de corectat
q detresa respiratorie marcata
q retractii severe
q apneea recurenta (cu nivele bune al teofilinei).
Ventilatia mecanica
Ventilatia mecanica este principala modalitate de terapie intensiva respiratorie utilizata la nou-nascutii cu insuficienta respiratorie moderata pana la severa sau in caz de insuficienta multiorganica. In ultimii 30 de ani s-au dezvoltat diferite tipuri de aparate de respiratie artificiala, fiecare cu avantajele si complicatiile sale pulmonare si cardiovasculare.
Experimentele recente pe modele animale adulte au demonstrat ca volumul insuflat in plamani prin ventilatie mecanica este principala variabila care determina afectarea pe termen lung a plamanilor, cunoscuta sub denumirea de displazia bronhopulmonara (DBP). Din aceste motive, termenul de "volubarotrauma" este utilizat frecvent pentru complicatiile pulmonare ale ventilatiei mecanice. Efectele cardiovasculare ale ventilatiei mecanice sunt determinate in special de presiunea end-expiratorie crescuta, rezultand o scadere a intoarcerii venoase si a debitului cardiac si perturbarea fluxului sanguin pulmonar. Perfectionarea aparatelor si a tehnicii de ventilatie au dus la scaderea complicatiilor postventilatorii.
Tipuri de aparate de ventilatie
Majoritatea aparatelor conventionale utilizate in asistenta nou nascutului sunt ciclice, cu presiune limitata si flux continuu. Aceste aparate permit continuarea respiratiei spontane in timpul fazei expiratorii a respiratiei. Aparatele de ventilatie se pot clasifica in: aparate de ventilatie conventionala si aparate de ventilatie cu frecventa inalta.
Ventilatia mecanica conventionala
Ventilatia mecanica intermitenta (IMV) sau ventilatia cu presiune pozitiva intermitenta (IPPV) - respiratii mecanice la intervale fixe cu respiratii spontane posibile intre ele.
Ventilatia mecanica intermitenta sincrona (SIMV)- respiratii mecanice cu rata fixa, dar initiate de efortul respirator al nou-nascutului.
Ventilatia mecanica declansata de pacient (PTV) - fiecare din miscarile respiratorii ale nou nascutului va declansa o respiratie mecanica la presiune si FiO2 prestabilite.
Ventilatia mecanica cu frecventa inalta:
Ventilatia oscilatorie de frecventa inalta (HFOV) - volumul tidal este realizat prin miscarea unei membrane sau a unui piston.
Ventilatia de frecventa inalta, in jet (HFJV)- volumul tidal este realizat prin propulsarea gazului printr-o canula cu diametru mic.
Ventilatie de frecventa inalta cu flux intermitent (HFFIV) - volumul tidal este produs prin flux pulsatil printr-o supapa pneumatica.
Ventilatia cu presiune pozitiva intermitenta (IPPV)
Indicatii
Indicatii absolute:
q colaps brusc cu apnee, bradicardie si esecul stabilirii unei respiratii satisfacatoare dupa o scurta perioada de ventilare cu balon si masca.
q esecul realizarii respiratiei spontane, adecvate in sala de nastere, dupa o resuscitare prompta si corecta. Prioritate au prematurii cu risc pentru RDS.
Indicatii relative:
q se aplica noilor nascuti cu respiratie spontana, dar care prezinta simptomele clinice sau gazometrice ale insuficientei respiratorii neonatale.
Tehnici IPPV si setarile ventilatorii
In prezent cea mai utilizata tehnica de ventilatie este ventilatia cu presiune pozitiva, presiune limitata, timp-controlata, frecventa conventionala, folosind un tub endotraheal.
Exista insa si anumite dezavantaje:
- intubarea prematurilor de grad mare poate fi dificila si cauza deteriorarea starii generale.
- laringoscopul poate leza cavitatea bucala, epiglota, laringele.
- prezenta tubului endotraheal poate provoca leziuni locale (imflamatie, eroziuni, ulcerari, vegetatii, stenoze).
- tubul plasat in faringe poate predispune la infectii locale, in special otita medie.
- tubul impins prea adanc in plamani (de obicei in bronhia principala dreapta) poate cauza supradistensia plamanului drept cu posibila aparitie a emfizemului interstitial sau a pneumotoraxului si colapsul cu atelectazia plamanului controlateral.
- tubul diminueaza mecanismele de 'clearance' ale plamanilor, favorizand astfel retentia secretiilor.
- daca tubul este prea mic, creste rezistanta caii aeriene, crescand astfel efortul respirator la copii cu CPAP sau frecvente ventilatorii scazute.
- efectele hemodinamice ale IPPV + PEEP pot duce la scaderea tensiunii arteriale si a fractiei de ejectie cardiaca.
- complicatiile majore ale IPPV sunt pneumotoraxul, DBP (displazia bronho-pulmonara), dezvoltarea unei hemoragii periventriculare si infectia. Toate aceste complicatii iatrogene pot fi cauze de deces la nou-nascutul pe IPPV.
In continuare vom descrie in detaliu tehnica ventilatia cu presiune pozitiva - limitata, timp controlata si frecventa conventionala.
Aparatul elibereaza (administreaza) un flux continuu de gaz, destinde plamanii la un timp inspirator (T insp) presetat la o presiune predeterminata. In timpul expirului, ventilatorul continua sa administreze fluxul de gaz pentru aplicarea presiunii pozitive end-expiratorii (PEEP), daca este necesar.
Gazul intra in plamani pe perioada timpului inspirator, cantitatea intrata fiind determinata de presiunea inspiratorie de varf (PIP) setata si de rata fluxului care trebuie sa fie suficient de ridicat pentru ca presiunea de varf presetata sa poata fi atinsa in timpul inspirator disponibil.
Cand presiunea dorita este atinsa, valva de limitare a presiunii se deschide, astfel se previne cresterea ei in continuare; cu cat timpul inspirator este mai lung, cu atat plamanii sunt mai mult timp destinsi la presiunea stabilita. Cu cat presiunea stabilita este mai mare, cu atat volumul de gaz intrat este mai mare, aceasta depinzand insa si de complianta plamanilor pentru ca in plamanii non-complianti se produce o 'scapare de aer' in jurul tubului endotraheal.
Presiunile inspiratorii de varf (peak inflating pressures=PIP)
PIP este o variabila importanta in determinarea volumului tidal si se stabileste in raport cu complianta pulmonara si rezistenta cailor respiratorii. PIP trebuie ajustata la excursiile toracice vizibile.
Presiunea trebuie sa fie suficient de mare pentru a obtine valori bune ale gazelor sanguine, dar presiunile mari pot produce pneumotorax (risc de volubarotrauma), deci trebuiesc alese presiunile cele mai mici posibile compatibile cu valorile normale ale gazelor sanguine. Dar daca PIP este prea joasa se poate dezvolta un sunt intrapulmonar.
In general, presiunile initiale la nou-nascutii cu afectare pulmonara (spre deosebire de cei cu apnee centrala si fara afectare pulmonara ) vor fi de 20 - 25 cm H2O. Hipoventilarea produce cresterea PaCO2 si scaderea PaO2 iar hiperventilarea scade PaCO2 si uneori PaO2 este excesiv de ridicata.
Presiunea pozitiva end-expiratorie (PEEP
Actioneaza (la fel ca si CPAP) prin mentinerea deschisa a cailor aeriene periferice, in timpul expirului, avand un rol important in cresterea capacitatii reziduale functionale si recrutarea ariilor atelectatice pentru schimbul gazos.
Valoarea la care trebuie mentinut PEEP pentru o buna oxigenare este de 5 cm H2O. Un PEEP mai mare, mai ales daca timpul de expir este scurt nu permite un expir complet la nivelul plamanilor, compromitand schimbul de gazela nivel alveolar.
In plus, avantajul PEEP, este ca ea conserva surfactantul de pe suprafata alveolara.
Presiunea medie din caile respiratorii (Mean Airway Presure=MAP)
MAP este un factor generat prin combinarea PIP,PEEP si a Tinsp.
Exista o buna corelare intre MAP si gradul oxigenarii copilului, ceea ce inseamna ca oxigenarea poate fi imbunatatita prin cresterea timpului inspirator, sau PEEP, sau PIP - ori combinatiile acestora. Dar trebuie pus in balanta "pretul" imbunatatirii oxigenarii cu riscul de volubarotrauma. Ideal MAP ar trebui sa fie mai mic de 10 cm H2O pentru reducerea la minim a riscului de volubarotrauma.
![]()
MAP = Tinsp/(Tinsp+Texp) x PIP + (1-Tinsp)/(Tinsp+Texp) x PEEP
Frecventa respiratorie
Studiile efectuate pana in prezent au aratat ca la o frecventa de 60 resp./minut, cu un Tinsp = 0,5 sec si presiuni scazute, se obtin valori mai bune ale gazelor sanguine decat la o frecventa de 30 resp/min. Prin cresterea frecventei la 75 - 100 resp/min se poate induce o respiratie sincrona cu aparatul la majoritatea nou-nascutilor. Frecventele mai mari (100 - 120 resp/minut) sunt lipsite de avantaje.
Timpul inspirator (Tinsp), timpul expirator (Texp), raportul inspir/expir (I:E), rata fluxul gazului inspirat
Experienta a dovedit ca in cazul ventilarii nou nascutilor cu SDR, Tinsp indicat este de 0,31 sec, Texp = 0,42 sec, cu un raport I:E = 1:1,3 la aceste setari obtinandu-se de obicei o respiratie a copilului sincrona cu aparatul.
Cresterea Tinsp poate perturba acest sincronism, scazand PaO2 si provocand 'reflex expirator activ' ceea ce duce la riscul producerii pneumotoraxului.
Un Tinsp. mai scurt (cum ar fi 0,3-0,4 sec) trebuie utilizat in perioada 'intarcarii' de aparat.
Rata fluxul gazului inspirat influenteaza MAP, prin influentarea timpului necesar atingerii PIP.
In practica, este utilizat un flux initial de 6-10l/min, dar la frecvente >100resp/min si PIP > 30 cmH2O, necesare in cazuri severe de boala, rata fluxului trebuie crescuta pana la 20l/min.
Probleme mecanice
La frecvente respiratorii mai mari de 80 - 100 resp/min scade volumul tidal (volumul curent) si minut-volumul, deci scade MAP, cu scaderea consecutiva a PaO2 si cresterea PaCO2, ceea ce se poate evita doar prin cresterea fluxului sau a PIP. Datorita constructiei aparatelor (care au incorporate valve expiratorii non-asistate - cum e cazul Drager Babylog) la aceste frecvente mai mari creste si PEEP-ul ceea ce reduce volumul tidal duce la retentie de CO2 si cresterea riscului de pneumotorax.
Probleme fiziologice
La frecvente respiratorii mari, Texp al ventilatorului poate fi mai scurt decat constanta de timp expiratorie a plamanului nou-nascutului, si astfel aerul se poate acumula realizand un PEEP -inadvertent (nedorit) de 2-3cmH2O. Blocarea de aer este o problema in special la copiii paralizati (medicamentos). La copiii paralizati cu VG<31saptamani, frecventa trebuie limitata la 60resp/min (Texp=0,5 sec).
Atitudinea ulterioara in timpul IPPV
Indiferent de afectiunea pulmonara. la copilul aflat pe IPPV este obligatorie determinarea gazelor sanguine. Setarile ventilatorii se vor modifica dupa aceste valori, dupa cum urmeaza:
|
SITUATIE |
ATITUDINE DE LUAT |
|
PaO2 scazut Pa CO2 crescut |
Creste PIP (ceea ce duce la MAP) La copilul care respira si spontan frecventei poate da rezultate bune |
|
PaO2 scazut PaCO2 normal |
FiO2 MAP dar mentine PIP ( ex: PEEP sau Tinsp) |
|
PaO2 scazut PaCO2 scazut |
Considera alt diagnostic: ex.PPHN, septicemie, supraventilare, FiO2, MAP; utilizeaza vasodilatatoare |
|
PaO2 normal PaCO2 crescut |
PEEP frecventa respiratorie mentine MAP constant |
|
PaO2 normal PaCO2 scazut |
frecventa respiratorie mentine MAP constant |
|
PaO2 crescut PaCO2 crescut |
Rara: verifica probleme mecanice (ex. obstruarea tubului) PEEP, Tinsp. frecventa respiratorie FiO2 |
|
PaO2 crescut PaCO2 normal |
MAP (de obicei PIP) FiO2 |
|
PaO2 crescut PaCO2 scazut |
presiunea frecventa respiratorie FiO2 |
|
PaO2 normal PaCO2 normal |
STAI LINISTIT! |
Indepartarea' sau 'intarcarea' de ventilator
Daca valorile gazelor sanguine sunt satisfacatoare (PaO2 = 60 -90 mmHg, PaCO2 < 42 - 49 mmHg, Ph > 7,25) si copilul a fost stabil, la aceste valori timp de 6 - 12 ore, se va incerca indepartarea de aparat. Exista riscuri mari in cazul scoaterii prea rapide de pe IPPV (a ventilarii prea scurte), in special la prematurii cu SDR < 36 de ore de la nastere, la care procesul prea rapid de indepartare poate duce la reaparitia atelectaziei severe fiind necesara o ventilatie si mai agresiva decat cea precedenta. Pe de alta parte, complicatiile IPPV cum ar fi infectia, DBP, 'scaparea' de aer sunt corelate cu durata IPPV, de aceea copilul trebuie detubat cat de rapid posibil.
In timpul indepartarii de aparat trebuie redus intai parametrul cel mai daunator. Astfel se reduce intai presiunea (PIP), apoi frecventa, FiO2 (in cazul administrarii de vasodilatatoare - acestea se opresc primele, cu exceptia HPPN). Reducerea PIP (factorul etiologic principal al pneumotoraxului si DBP) este usoara in SDR sau aspiratia de meconiu, atat de rapid pe cat permit gazele sanguine, dar trebuie redus cu mare grija in HPPN.
Odata ce am redus PIP la 25cmH2O, avand inca o frecventa de 60-80 resp/min la FiO2 = 80-90 , in continuare frecventa, FiO2 si PIP + PEEP pot fi reduse simultan, scazand frecventa si presiunea daca PaCO2 este bine controlata sau avem alcaloza respiratorie. Presiunea si oxigenul se scad daca PaO2 este >60-68mmHg.
In general, setarile se reduc in trepte mici:
pentru FiO2
- 5 - 10resp/min in cazul frecventei respiratorii
- 2/3 cmH2O pentru PIP
Daca se reduc prea rapid, in trepte prea mari, nou nascutul poate deveni hipoxic si hipercapnic. Dupa fiecare modificare, se controleaza gazele in decurs de 30 minute.
In cazul utilizarii de pancuronium sau fentanyl, nu intrerupem administrarea pana ce nu sunt rezolvate problemele legate de 'scaparile' de aer si setarile au fost reduse la 22-25/5 cmH2O, 40-50resp/min si FiO2 50-60
Cand copilul prezinta eforturi respiratorii spontane si presiunile au fost reduse la 16-18/3 cmH2O, frecventa se reduce in trepte initiale de 5-10 resp/min apoi in trepte de 2-5resp/min pana cand am ajuns la frecvente de sub 20 resp/min, cu speranta ca nou-nascutul va respira spontan, fiind mentinut de insuflarile ventilatorii. In aceasta faza, utilizarea unui Tinsp scurt de 0,5 sec, permite o indepartare mai rapida. In aceste ultime etape, nu e nevoie sa asteptam ca gazele sa fie 'perfecte'; daca ele sunt acceptabile, setarile se reduc la fiecare 6-8 ore, si se observa daca nou-nascutul poate mentine gazele in cursul reducerii IPPV. Daca da, este foarte probabil ca exturbarea sa se poata realiza cu succes.
Cand nou nascutul este la FiO2 40 , presiuni de 16/2-3 cmH2O si frecventa 10 resp/min, de obicei va tolera CPAP si poate fi extubat. Initial CPAP poate fi incercat pe tubul endotraheal. Totusi, respirarea spontana printr-un tub ingust creste efortul respirator si copilul se poate epuiza usor, lasandu-l pe CPAP mai mult de 1-2h si reducand posibilul succes al detubarii. De aceea, dupa doar 1-2 ore de CPAP endotraheal, cu gazele normale, trebuie detubat si conectat la CPAP nazal, de obicei la acelasi FiO2 si presiune de 3-5cmH2O. Uneori poate fi utila cresterea FiO2 cu 5-10 (cu monitorizarea PaO2), pentru sustinerea oxigenarii imediat dupa extubare.
La majoritatea nou-nascutilor, CPAP nazal poate fi redus in urmatoarele 48-72 ore si apoi intrerupt, punand copilul in izoleta la 30-40 O2. Cu toate acestea, in special la prematuri, CPAP nazal trebuie continuat uneori timp de mai multe zile sau saptamani pentru prevenirea atacurilor de apnee, recurente.
La nou nascutii cu GN>1500g, indepartarea poate fi rapida - in decurs de 12-24 ore, fara a fi necesare perioade mai lungi de ventilare lenta sau CPAP nazal.
Din contra, la nou-nascutii cu GN < 1000 - 1250 g, ultimele etape ale indepartarii pot dura saptamani. La majoritatea nou-nascutilor cu GN <1500 g si VG<32 saptamani de gestatie, se recomanda aminofilina sau teofilina iv. 5mg/Kg/24 ore, cu 48-72 ore inainte de probabila detubare.
Probleme legate de indepartare
Rareori secventa de mai sus, care culmineaza cu extubarea si plasarea copilului sub izoleta, se desfasoara dupa un curs fara probleme. Dupa fiecare treapta, copilul se poate agrava clinic, sau gazele sanguine la noua setare pot deveni inacceptabile. Un semn care sugereaza ca procesul indepartarii nu progreseaza, in special la prematurii cu greutate mica, este dezvoltarea dupa 6-12 ore a unei acidoze metabolice, probabil semn al unui efort respirator excesiv, la noua setare ventilatorie. In aceste situatii (si dupa verificarea ca nu avem de a face cu obturarea tubului sau un pneumotorax) se revine la setarea precedenta. Cu toate acestea, la unii copii, dupa deteriorare, e nevoie de o ventilare si mai riguroasa pentru 24-48 ore, inaintea reinceperii intregului proces al indepartarii. Criteriile pentru reintubare sunt identice cu cele ale intubarii in sine.
Extubarea
Elementul principal si irevocabil in procesul indepartarii este detubarea care nu numai ca poate fi prematura, dar comporta si riscul de hipoxie severa ce poate duce la HMC, inhalarea de continut gastric si necesitatea reintubarii cu riscurile de leziuni laringiene. De aceea este esential sa tentam extubarea doar la copilul aflat in starea cea mai buna posibila, incluzand electrolitii normali, Hb 14g si status acido-bazic normal.
Alimentatia trebuie intrerupta cu 6-12 ore inaintea detubarii si nu se reia pentru inca 24 ore, pentru ca riscul regurgitarii si aspiratiei sa fie minim.
Dupa detubare, nou nascutul prezinta deseori dificultati in evacuarea secretiilor (clearace-ul cailor aeriene este compromis de leziunile produse de tub). De aceea, oxigenul inspirat trebuie umidificat si incalzit corespunzator. Fizioterapia si aspiratia orofaringiana regulata trebuie inceputa, dar efectuata de asemenea maniera incat sa nu produca deteriorari ale gazelor sanguine sau apnee cu bradicardie. In general, ambele se efectueaza odata la 3-4 ore, crescand sau scazand frecventa lor in functie de starea clinica si grafia toracica.
La fel ca la nou nascutul ce respira spontan si la cel ventilat, ingrijirea in decubit ventral duce la valori mai bune ale gazelor sanguine.
Probleme legate de extubare
Stridorul - un stridor minim este obisnuit, avand o durata, de obicei, de 1 - 2 ore, maxim 24 ore. Daca este persistent, se poate administra CPAP nazal sau nazo-faringian la presiune mai mare (ex. 8-10 cmH2O, la fel ca si in problemele laringiene congenitale). Daca stridorul este marcat si apare detresa respiratorie cu alterarea gazelor, nu exista alta alternativa decat reintubarea. La acesti pacienti se utilizeaza tub endotraheal, pe calea nazala si se lasa copilul pe CPAP sau ventilatie minima pentru minim 2-3 zile inaintea tentarii detubarii si dupa ce s-a administrat cu 24 de ore inaintea detubarii si inca 24-48 ore dupa detubare, dexametazona 0,5 mg/Kg.
Colapsul lobar
In ciuda fizioterapiei si a aspiratiei adecvate dupa detubare 25 % din nou-nascutii detubati dezvolta colapsul unui plaman, sau doar al unui lob - de obicei lobul superior drept, din cauza obstruarii bronsiilor cu secretii (acest fenomen pare sa fie mai frecvent dupa intubarea nazala). Acesta poate sa produca o asemenea deteriorare incat sa fie necesara reintubarea +IPPV. La alti nou-nascuti deteriorarea este mai putin dramatica, fiind chiar asimptomatica. Aceste cazuri de gravitate medie se trateaza cu fizioterapie riguroasa. Uneori, este necesara aspirarea cailor aeriene, sub ghidare laringoscopica directa (intorcand capul in partea opusa plamanului afectat, cateterul se introduce in bronsia principala respectiva).
Pentru a detecta ariile de colaps, in special cele ale lobului superior drept inainte sa progreseze pana la colaps pulmonar total, la toti nou-nascutii detubati se efectueaza o radiografie pulmonara in decurs de 24-48 ore de la detubare, sau ori de cate ori exista o deteriorare a starii clinice sau a gazelor sanguine.
Esecul recurent al" indepartarii" sau detubarii
Cu exceptia cazurilor cand s-a produs o leziune laringiana, incercarile repetate, fara succes, de detubare a unui nou-nascut timp de o saptamana, reprezinta o problema doar la cei cu greutate foarte mica, a caror greutate nu creste si la care episoadele repetate de detubare si deteriorare fac si mai grea o nutritie adecvata. O alta cauza a esecului este leziunea neurologica, secundara unei hemoragii periventriculare. Ambele categorii de copii se reintubeaza pe cale nazala, se reincepe IPPV la o frecventa de 5-10 resp/min, cu mentinerea ventilatiei pentru 7-10 zile si alimentatie corespunzatoare pana ce ajung intr-o stare mai buna, cu nivel optim de teofilina si cu 100-200g mai mult in greutate. Esecul repetat al indepartarii de IPPV unui nou-nascut anabolic este sugestiv pentru o problema neurologica primara sau secundara HMC.
Ventilatia cu frecventa inalta (HFV)
HFV este tehnica folosita in starile critice din neonatologie, in special dupa ce ventilatia conventionala a esuat. HFV poate reduce incidenta sindroamelor de "scurgere" a aerului si a bolilor cronice pulmonare la nou-nascutii prematuri, reduce necesarul oxigenarii prin membrana extracorporeala la nou-nascutul la termen. HFV utilizeaza frecvente ventilatorii cuprinse intre 4-22 Hz, o MAP inalta si un volum tidal mai mic decat cel fiziologic. Acest volum tidal mic este eliberat intr-un ritm extrem de rapid, generand vibratii si curenti care faciliteaza schimbul gazos. Debitul ventilator este determinat prin cresterea amplitudinii oscilatiilor. Ca rezultat al MAP inalte alveolele colabate sunt recrutate si, astfel, capacitatea reziduala functionala crescuta determina cresterea interfetei alveolo-arteriala si, consecutiv, imbogatirea schimbului gazos; rezultand o ventilatie alveolara mai buna.
HFV poate fi impartita in trei categorii in functie de procedeul utilizat si de mecanismul de baza al ventilatiei:
HFOV utilizeaza o frecventa de la 5 la 50 Hz ( pana la 3000 cicli/min.), inspirul si expirul sunt active si volumul tidal este de marimea spatiului mort. Se crede ca eficacitatea unui asemenea volum tidal este data de amestecul bun realizat in caile aeriene si plamani intre aerul proaspat inspirat si cel expirat.
HFJV se bazeaza pe o sursa suplimentara de presiune inalta. Aceste aparate emit debite inspiratorii mici cu o frecventa de 4-10 Hz (150-600 cicli/min), inspirul este activ, iar expirul este pasiv.
HFFIV utilizeaza valve pneumatice controlate prin microprocesoare sau bile pneumatice pentru a intrerupe sursa de gaz presurizat, creand astfel un flux pulsatil. Frecventele utilizate in aceasta metoda sunt intre 10-15 Hz (300-900 cicli/min.), inspirul este activ, iar expirul este pasiv.
In timp ce majoritatea neonatalogilor recomanda utilizarea HFV ca terapie "de salvare" la pacientii tratati initial cu ventilatie conventionala, experimentele mai recente sugereaza ca utilizarea precoce a HFOV este benefica. Keszler si col. au demonstrat prin studii multicentrice ca nou-nascutii, in special cei cu emfizem pulmonar interstitial, au raspuns favorabil si au avut o rata mai buna de supravietuire cu HFV in comparatie cu ventilatia conventionala. HFV imbunatateste schimbul gazos la cele mai mici presiuni medii si de varf in caile aeriene. HFV a fost asociata cu o rezolutie mai rapida a emfizemului pulmonar.
In unele studii incidenta hemoragiei intraventriculare si a leucomalaciei periventriculare a fost semnificativ mai mare in grupul HFV comparativ cu ventilatia conventionala.In contrast cu aceste rezultate, in alte studii incidenta hemoragiei intraventriculare nu a fost crescuta, dar populatia studiata a fost oarecum diferita.
Surfactantul
Surfactantul este o molecula fosfolipidica unica care scade tensiunea superficiala in alveole si imbunatateste fluxul sanguin pulmonar. Disfunctia surfactantului poate fi determinata de deficitul surfactantului sau al uneia din componentele sale, asa cum se intampla in SDR, sau de deficitul congenital de proteina B sau inactivarea surfactantului, ca in sindromul de aspiratie meconiala. Astazi exista doua tipuri majore de surfactant exogen (sintetic) sau natural (prelucrat din plaman de vaca, porc sau din lichid amniotic uman ). Utilizarea tuturor tipurilor de surfactant in tratamentul nou-nascutilor prematuri scade mortalitatea si morbiditatea prin SDR si, scade, de asemenea, incidenta acestui sindrom.
Indicatiile administrarii surfactantului- conform Institutului pentru Ocrotirea Mamei si Copilului- Bucuresti
- profilactic: prematuri sub 32 de saptamani
- terapeutic: prematuri si nou-nascuti la termen cu SDR
Studiile arata ca exista diferente clinice privind promptitudinea raspunsului, realizandu-se o eficacitate terapeutica mai mare prin utilizarea surfactantului natural decat a celui sintetic. Un studiu comparativ privind cele doua categorii de surfactant la 1296 prematuri cantarind intre 501 si 1500 grame nu a aratat diferente privind incidenta deceselor sau a bolilor cronice pulmonare la 28 de zile de viata, dar a existat o imbunatatire semnificativa a evolutiei clinice secundare, demonstrand ca Survanta (surfactant natural) este mai eficient decat Exosulf (surfactant sintetic).
In subgrupul nou-nascutilor cu greutatea intre 1001 si 1500 grame, copiii tratati cu surfactant natural au avut o rata semnificativ mai mica a bolilor cronice pulmonare la varsta de 28 de zile, un necesar mai mic pentru suplimentarea oxigenului si o MAP mai mica la 6 si 72 de ore dupa ce surfactantul a fost instilat pe tubul endotraheal. Nu a existat nici o alta diferenta intre cele doua grupuri privind incidenta altor complicatii neonatale. Arnold si col. au comparat surfactantul natural cu cel sintetic si nu au gasit diferente semnificative privind succesul extubatiei si al discontinuitatii terapiei cu oxigen intre cele doua substante. In grupul surfactantului natural a fost observat un raspuns initial mai rapid masurat prin FiO2 si MAP. Aceasta diferenta privind intervalul de raspuns se datoreaza lipsei proteinelor B si C din surfactantul sintetic.
Doza initiala in terapia de substitutie, care este administrata de obicei in cazuri grave, trebuie administrata pe tubul endotraheal cat mai aproape posibil de momentul alterarii starii copilului. Un alt studiu sustine utilizarea surfactantului inhalat prin CPAP nazala cat mai devreme posibil pentru a preveni progresia insuficientei respiratorii si a scadea nevoia de intubare endotraheala. Sunt necesare mai multe studii pentru a dovedi eficacitatea surfactantului inhalat inaintea instituirii acestor noi metode.
Ventilatia lichida
Ventilatia lichida consta in insuflarea in plamani a unui lichid perfluorocarbonat oxigenat care sustine schimbul gazos fiziologic.
Lichidele de perfluorocarbon (PFC) sunt clare, inodore, netoxice, stabile chimic, sunt lichide biocompatibile care au o tensiune de suprafata scazuta si o solubilitate crescuta pentru oxigen. Lichidele PFC permit oxigenarea adecvata si indepartarea CO2 la presiuni scazute de inflatie raportat la ventilatia gazoasa a plamanului imatur sau afectat. Nu s-au raportat efecte adverse morfologice sau biochimice la nivel pulmonar, dupa ventilatia lichida cu PFC. Se produce numai o absorbtie la nivelul capilarelor pulmonare a lichidului PFC. S-a demonstrat pe modelele animale ca ventilatia lichida este eficienta in mentinerea sau imbunatatirea schimbului gazos la presiuni mici de inflatie.
Aceste presiuni scazute au fost realizate in ciuda rezistentei crescute in caile aeriene, care a fost crescuta prin densitatea si vascozitatea PFC. Spre deosebire de plamanul inflatat cu aer, in care presiunile alveolare nu sunt uniforme si presiunile vasculare sunt subiectul de variatie al gradientelor hidrostatice, plamanul inflatat cu lichid prezinta un gradient transmural care prezinta un echilibru relativ. Fluxul sanguin pulmonar este distribuit mai regulat in plamanul inflatat cu lichid, rezultand o ameliorare a echilibrului ventilatie-perfuzie, o stabilitate alveolara mai mare si o scadere a suntului intrapulmonar si a atelectaziei.
S-a demonstrat pe modele animale ca avantajul ventilatiei lichide persista si dupa ce tratamentul a fost intrerupt. Complianta pulmonara si gradientul de oxigen arterial alveolar sunt mai bune dupa ventilatia lichida in comparatie cu cea gazoasa. Mentinerea unei presiuni de inflatie reduse determina mai putin probabil aparitia unor complicatii ca pneumotoraxul si instabilitatea cardiopulmonara.
Ventilatia lichida poate fi utila in insuficienta respiratorie de alte cauze decat deficitul de surfactant. In sindromul de aspiratie ( modele animale ) oxigenarea si complianta pulmonara au fost imbunatatite in timpul si dupa ventilatia lichida, probabil prin lavajul arborelui traheo-bronsic precum si prin instituirea ventilatiei si perfuziei mai bune.
Alte aspecte studiate ale ventilatiei lichide includ utilizarea altor tipuri de ventilatie decat ventilatia pura. Deoarece lichidul este distribuit omogen in plamani el poate fi utilizat pentru a oferi factori biochimici direct la nivel pulmonar. Administrarea pulmonara de Tolazolin a fost studiata pe un model de miel. Daca se compara cu administrarea intravenoasa se observa o scadere mai mare a presiunii medii pulmonare, cu o scadere mai mica a presiunii medii sistemice si imbunatatirea oxigenarii. Lichidele PFC realizeaza un mediu de contrast excelent. Exista o potrivire unica cu functiile organului monitorizat, cu mecanismele biochimice si masurile terapeutice, furnizand un mod de evaluare a ventilatiei si perfuziei in relatie cu structura anatomica. Atenuarea acustica a PFC face din el un excelent mediu pentru vizualizarea structurii pulmonare cu tehnologie ultraperformanta.
PFC poate fi instilat printr-un tub endotraheal sau de traheostomie. Sistemul asistat mecanic este un aparat de by-pass inima-plamani modificat. Sistemul ventilator cu lichid poate fi reglat ca si aparatele de ventilatie conventionala la care volumul tidal, frecventa, rata inspiratorie si expiratorie si fluxul lichid pot fi ajustate. Timpii inspirator si expirator, sunt controlati de valve si activati de un ceas. Volumul tidal si capacitatea reziduala functionala sunt monitorizate cu un cantar de pat care masoara diferenta de greutate cand lichidul curge afara. Capacitatea reziduala functionala a fost apreciata la aproximativ 30 ml/kg, iar volumul tidal la aproximativ 15 ml/kg. Presiunea partiala a oxigenului inspirat poate fi reglata prin procentul de oxigen circulant prin membrana de oxigenare. Nivelul dioxidului de carbon poate fi reglat prin variatia ratei fluxului lichid ce trece prin membrana. S-a demonstrat ca cea mai eficienta eliminare a CO2 se produce la o frecventa respiratorie mica (5-9 resp/min) ca rezultat al timpului de difuziune crescut.
Prima experienta umana a ventilatiei lichide a fost raportata in 1990. Cea mai recenta aplicatie a acestei tehnici este utilizarea combinata a ventilatiei lichide, care realizeaza umplerea plamanului si sustinerea capacitatii reziduale functionale prin lichidul PFC, cu cea gazoasa conventionala, simultan. Ventilatia lichida este mai putin invaziva decat ECMO si duce la riscuri mai mici. Ea poate facilita recuperarea pulmonara prin mobilizarea secretiilor, recrutarea zonelor atelectazice si cresterea fluxului sanguin regional. Este de asemenea studiata posibilitatea de alternativa pentru ECMO la cei care nu raspund la aceasta terapie. Ventilatia lichida pare sa fie o alternativa sigura si eficienta, dar, totusi, trebuiesc luate precautii pentru viitoarele experiente.
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2024 - Toate drepturile rezervate -| |
|
|
|||
|
|||
|
|||
Analize pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||








