
| Biologie | Botanica | Chimie | Didactica | Fizica | Geografie |
| Gradinita | Literatura | Matematica |
Chimie
|
|
Qdidactic » didactica & scoala » chimie Metode de investigare a reactiilor la electrod |
Metode de investigare a reactiilor la electrod
Metode de investigare a reactiilor la electrod
3.1.Voltametria ciclica
Voltametria este printre cele mai utilizate metode electrochimice de investigare, oferind informatii despre speciile electroactive implicate in procesele electrochimice, despre cuplarea etapelor chimice cu etape electrochimice, despre fenomenul de electrosorbtie, precum si alte date cinetice privind procesul studiat. Metoda se bazeaza pe urmarirea raspunsului de curent pe care il da elecrodul studiat, din solutia aflata in repaus si al carui potential este modificat liniar, (voltametrie liniara) sau ciclic (voltametrie ciclica).
Semnalul de excitare in voltametria ciclica consta in baleiajul de potential avand forma triunghiulara.
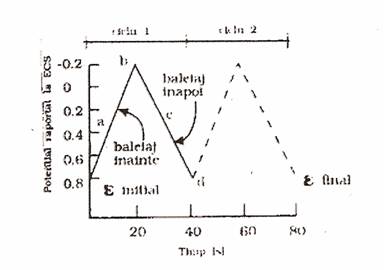
Fig. 6 Semnalul de excitare in VOC
Parametrii importanti ai unei voltamograme ciclice pentru un sistem reversibil sunt:
- curentul de varf (anodic respectiv catodic) Ia,v; Ic,v (echivalentul curentului limita din polarografia clasica)
- potentialele de varf (anodic respectiv catodic) ε a,v ; ε c,v (pentru sisteme reversibile, pozitia lor nu depinde de viteza de baleiaj)
- potentialul formal definit pentru un cuplu reversibil
- distanta intre potentialele de varf (Δεv) care permite determinarea numarului de electroni z schimbati (in cazul proceselor reversibile).
Acest raport poate fi puternic influentat de etapele chimice cuplate cu etapa de transfer de sarcina.
Ireversibilitatea electrochimica este generata de un schimb lent de electroni la electrodul de studiat (i0 mic) si, in aceste cazuri, relatiile pentru calculul z, Iv de la sistemele reversibile nu sunt valabile. O voltamograma pentru un astfel de sistem ireversibil este prezentata in fig 7 .
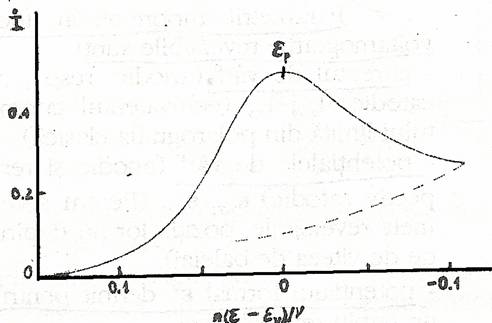
Fig . 7. Voltamograma ciclica a unui sistem ireversibil
Curentul de varf, in A este dat de expresia :
Ic,v = -2.99 105 z ( c n)1/2 S c D0 1/2 v1/2
in care z este numarul total de electroni schimbati; αc - coeficientul de transfer polielectronic in sens catodic; n- numarul de electroni transferati in etapa determinanta de viteza; S - suprafata electrodului; c - concentratia speciei electroactive in faza de volum; D - coeficientul de difuzie a speciei care se reduce si v - viteza de baleiaj.
Pentru sisteme cuasireversibile tratamentul matematic al ecuatiilor care descriu forma voltamogramelor, este mai complex. Exista insa solutii numerice[4].
I. Partea experimentala
Introducere
In acest context[L1] , lucrarea de fata isi propune sa studieze detectia urmelor de Cu din solutii apoase folosind electrozi modificati cu indigo carmin.
[L1]De precizat contextul
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2025 - Toate drepturile rezervate -| |
|
|
|||
|
|||
Lucrari pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||








