
| Biologie | Botanica | Chimie | Didactica | Fizica | Geografie |
| Gradinita | Literatura | Matematica |
Chimie
|
|
Qdidactic » didactica & scoala » chimie Reactii specifice unor acizi carboxilici |
Reactii specifice unor acizi carboxilici
REACTII SPECIFICE UNOR ACIZI CARBOXILICI
1. Acizi monocarboxilici saturati
Acidul formic HCOOH, este unul din putinii acizi cu caracter reducator:
![]()
a) Reactia cu fericianura (caracter reducator). Intr-o eprubeta cu 1-2 mL solutie de acid formic se introduc 2 picaturi de HCl 10% si o bucatica de magneziu. Dupa 5-6 minute de efervescenta, se adauga 3-4 picaturi solutie 5% de fericianura de potasiu, 2-4 picaturi solutie 0,5% fenilhidrazina si putin HCl conc. Apare o coloratie roz-rosie specifica HCOOH.
b) Reducerea azotatului de argint amoniacal. Intr-o eprubeta se prepara 1 mL reactiv Tollens. Se adauga 1 mL solutie de acid formic si se incalzeste pe baie de apa la fierbere. Apare un precipitat brun de argint:
HCOOH + 2Ag[(NH3)2]OH 2Ag + CO2 + 2H2O + 4NH3
c) Decolorarea solutiei de permanganat in mediu bazic. Peste 1 mL solutie de acid formic alcalinizata cu NaOH 5%, se adauga solutie KMnO4 0,1N. Disparitia culorii roz este dovada oxidarii acidului.
HCOOH + 2KMnO4 + 2KOH 2K2MnO4 + CO2 + 2H2O
Acidul acetic este cel mai important acid saturat monocarboxilic.
a) Formarea acetatului feric hidrolizabil. Intr-o eprubeta se neutralizeaza 1 mL solutie 1 N de acid acetic cu NaOH 1 N (se poate folosi direct acetat de sodiu). Peste solutie se adauga 6-8 picaturi FeCl3 1%. Continutul eprubetei se fierbe 2-3 minute cand apare un precipitat maron-roscat, de acetat feric.
b) Reactia cu furfurolul. Acidul acetic faciliteaza aminoliza furfuralului in prezenta anilinei cu formarea rosului de anil, un compus colorat intens in rosu-visiniu. Reactia este descrisa la furfurol si serveste pentru identificare si dozare. Inlocuind anilina cu benzidina (H2N-C6H4-C6H4-NH2), se poate diferentia acidul formic de acid acetic.
Astfel, in doua eprubete se adauga cate 1 mL solutie de acid formic si acid acetic. Peste fiecare se adauga cateva picaturi anilina sau cateva cristale benzidina si o picatura de solutie saturata de furfural. In eprubeta cu acid formic apare o coloratie galbena, iar in cealalta, rosu-violet.
Acidul benzoic este un acid slab, dar ceva mai tare ca acidul acetic.
a) Transformarea in acid salicilic. Peste 1 mL solutie de acid benzoic se adauga 0,2 mL acid acetic in apa 1:5 si 2,5 mL H2O2 30%. Eprubeta se mentine pe baie de apa la fierbere o ora. Reactia se accelereaza cu un cristal de sulfat feric drept catalizator. Dupa racire, proba se extrage cu 5 mL benzen; solventul se evapora in nisa si peste o portiune de reziduu se adauga o picatura de FeCl3 1%. Aparitia culorii violet confirma formarea salicilatului feric.
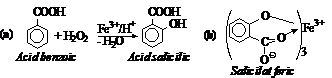
Reactia serveste la dozarea acidului benzoic in produse industriale.
2. Acizi carboxilici nesaturati
Acidul sorbic (acid hexan-2,4-dienoic: CH3-CH=CH-CH=CH-COOH).
a) Reactia cu a-naftol. O solutie diluata de acid sorbic (sub 0,1%) se trateaza cu o solutie de a-naftol (cateva cristale a-naftol dizolvat in H2SO4 conc.). Prin incalzire la 100 C apare o culoare rosie specifica.
|
b) Reactia cu acidul 2-tiobarbituric. Peste 1 mL proba cu acid sorbic se adauga 2 mL H2SO4 2 N si 1-2 mL solutie K2Cr2O7 0,01 N. Amestecul se incalzeste sub agitare pe baie de apa la fierbere 5-10 min. Se adauga 2-3 picaturi de acid 2-tiobarbituric 0,1% si se incalzeste inca 5-10 min. Aparitia unei coloratii rosii este dovada condensarii dialdehidei malonice dupa reactiile 8.25.
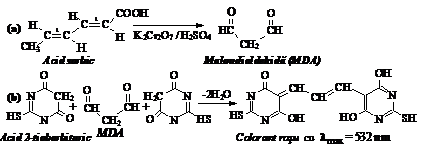
3. Reactii ale acizilor di- si policarboxilici
Acidul oxalic (HOOC-COOH)
a) Identificarea sub forma de oxalat de calciu. Acidul oxalic precipita cantitativ cu ionii de calciu in mediu neutru sau amoniacal. Intr-o eprubeta cu 1 mL solutie CaCl2 2 N se adauga o picatura din solutia de acid oxalic. Precipita oxalat de calciu alb. Precipitatul se filtreaza si se dizolva pe filtru in H2SO4 2%. Adaugand in solutie cateva picaturi de KMnO4 0,1 N, acesta se decoloreaza (deosebire de cei mai multi acizi carboxilici). Precipitarea ca sare de calciu este si o metoda de dozare gravimetrica a acidului oxalic. Mai utila este titrarea cu KMnO4 0,1 N a oxalatului de calciu sau a acidului oxalic in H2SO4 2%, conform reactiilor:
![]()
b) Reactia cu difenilamina. Un cristal de acid oxalic sau se topeste cu un cristal de difenilamina (Foarte toxica!!). Peste topitura racita se adauga 1 mL acid acetic. Apare coloratia albastra specifica produsilor transpozitiei benzidinice.
Acidul succinic (HOOC-CH2-CH2-COOH).
a) Identificarea cu p-N-dimetilamino-benzaldehida. Cateva mg de proba sau o picatura din solutia de analizat se incalzesc intr-o eprubeta cu 2-5 mg pulbere de zinc si o picatura NH4Cl 0,5%, la sec. La gura eprubetei se fixeaza o hartie de filtru impregnata cu solutie 5% de p-N(dimetil)amino-benzaldehida preparata in solutie benzenica de acid tricloracetic 20%. Partea de jos a eprubetei se incalzeste puternic. Vaporii ce se degaja coloreaza hartia in roz si apoi in rosu-violet (formare de pirol; sensibilitatea reactiei 0,5 mg acid succinic).
Acidul ftalic
a) Reactia de transformare in fluoresceina. Se topesc cateva cristale acid orto-ftalic si rezorcina cu cateva picaturi H2SO4 conc. Amestecul se incalzeste la flacara pana cand nu se mai degaja vapori de apa. Se raceste si se neutralizeaza cu NaOH 10-20%, observand aceeasi fluorescenta verzuie datorita sarii de sodiu a fluoresceinei.
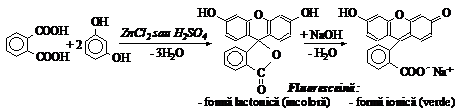
REACTII DE IDENTIFICARE PENTRU DERIVATII FUNCTIONALI AI ACIZILOR CARBOXILICI
1. Reactii de identificare pentru esteri
a) Saponificarea esterilor. Saponificarea este reactia inversa esterificarii. Are loc in mediu bazic cu formarea sapunurilor acizilor grasi (R-COO-Me+).
Cateva picaturi de ester se fierb cu exces de solutie NaOH 10%. Dupa racire si acidulare cu solutie HCl 10% acidul sau alcoolul format se vor identifica prin reactii caracteristice.
![]()
b) Transformarea esterilor in acizi hidroxamici. Se amesteca cateva picaturi ester cu 0,5-1 mL solutie metanolica 1 N de clorhidrat de hidroxilamina (NH2-OH HCl) si se adauga 2-3 picaturi timolftaleina (indicator de pH). Se adauga incet solutie metanolica de KOH 2 N pana apare coloratia albastra. Se adauga 3-5 picaturi de KOH in exces, se incalzeste scurt timp si se raceste. Se neutralizeaza KOH cu HCl 2 N pana dispare culoarea albastra a timolftaleinei. La adausul unei picaturi de FeCl3 10% apare culoarea rosie a hidroxamatului feric.
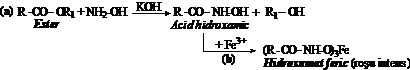
Reactia este utila si pentru dozarea spectrofotometrica a esterilor.
2. Reactii de identificare pentru amide si imide
a) Saponificarea amidelor. Amidele simple degaja prin saponificare (hidroliza bazica) la cald, amoniac ce se recunoaste dupa miros sau prin reactie cu hartie de filtru imbibata in reactiv Nessler (K2[HgI4]), iar amidele N-substituite pun in libertate amine ce se dizolva sau se extrag intr-un solvent potrivit. Reactiile se desfasoara potrivit ecuatiilor:
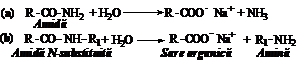
Cateva picaturi din solutia amidei se trateaza cu 1 mL NaOH 10%. NH3 degajat se identifica dupa miros sau dupa pata neagra sau bruna lasata pe o hartie de filtru impregnata cu Hg2(NO3)2 sau K2[HgI4].
b) Diferentierea amidelor acizilor aromatici de cele ale acizilor alifatici. La baza metodei sta transformarea in acizi hidroxamici. Cu deosebirea ca amidele acizilor aromatici de forma Ar-CONH2 se oxideaza la cald cu H2O2 pana la acizi hidroxamici, pe cand cele alifatice, R-CONH2, formeaza acizi hidroxamici prin condensare cu hidroxilamina in mediu alcoolic, ca si esterii.
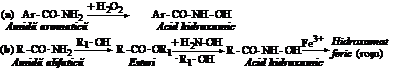
La suspensia sau solutia apoasa a 50 mg amida aromatica nesubstituita la azot se adauga 3-5 picaturi de H2O2 6% si se incalzeste pana la dizolvare completa sau pana nu se mai degaja oxigen. Dupa racirea solutiei, se adauga o picatura de FeCl3 5%. In scurt timp apare o coloratie albastra-rosie, la rece sau dupa usoara incalzire.
In paralel, 50 mg amida alifatica se trateaza cu 1 mL solutie alcoolica saturata de NH2-OH HCl. Se incalzeste 3 minute si dupa racire se adauga 1-2 picaturi FeCl3 5%. Apare culoarea rosie specifica.
c) Reactii pentru uree
Ureea se descompune la incalzire la peste 160 C in CO2, NH3 si biuret. Fiecare din acesti compusi se identifica separat.
Ureea formeaza saruri cu cate un singur echivalent de acid azotic sau oxalic:
H2N-CO-NH HNO3 H2N-CO-NH (COOH)2
Azotat de uree Oxalat de uree
3. Reactii de identificare pentru anhidride
a) Transformarea in alti derivati functionali. Anhidridele acizilor carboxilici reactioneaza cu alcooli, fenoxizi, amoniac si amine, trecand in esteri, amide, amide N-substituite si imide, substante cu Tf si Tt bine cunoscute, care permit identificarea lor.
b) Transformarea in acizi hidroxamici. Reactia este comuna cu cea de la esteri si amide. Acizii hidroxamici formati intermediar dau coloratii intense cu FeCl3.
Calitativ, intr-un pahar se introduc cateva picaturi sau cristale de anhidrida si cateva picaturi de solutie NH2OH HCl; amestecul se incalzeste usor, sub agitare. Se degaja abundent HCl. In final, amestecul se raceste si se neutralizeaza cu Na2CO3 10%. Solutia rezultata se poate folosi pentru identificarea acidului hidroxamic format prin reactii calitative cu clorura ferica, cand apare coloratia roz - violet a hidroxamatului feric ca la esteri, sau pentru reactii de precipitare cu acetat de plumb sau de cupru a hidroxamatului verde de Pb sau Cu.
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2025 - Toate drepturile rezervate -| |
|
|
|||
|
|||
Documente online pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||








