| Biologie | Botanica | Chimie | Didactica | Fizica | Geografie |
| Gradinita | Literatura | Matematica |
Chimie
|
|
Qdidactic » didactica & scoala » chimie Reactii pentru compusi cu functiuni simple azotate |
Reactii pentru compusi cu functiuni simple azotate
REACTII PENTRU COMPUSI CU FUNCTIUNI SIMPLE AZOTATE
1. Reactii de identificare a nitroderivatilor
1. Reactii pentru nitroderivatii alifatici.
a. Reactia Konovalov. Nitroderivatii primari si secundari (alifatici, pentru ca cei aromatici sunt numai tertiari), formeaza cu alcaliile acinitro-derivati care dau coloratii cu solutia apoasa de FeCl3 10%. La tratare cu HCl se revine la forma nitro.
|
|
Cateva picaturi de nitroderivat primar sau secundar se dizolva in 2-3 picaturi de metanol si se adauga o picatura de NaOH 20%. Dupa un repaus de 15 minute se aciduleaza slab cu HCl 10% si se adauga o picatura de FeCl3 10%. Solutia se coloreaza in rosu sau rosu-brun.
2. Reactiile nitroderivatilor aromatici
a. Reactia Ianovsky permite diferentierea polinitroderivatilor aromatici pe baza reactiei lor cu acetona (sau alte aldehide si cetone) in alcalii. Astfel, s-a constatat ca o-dinitroderivatii nu dau reactia Ianovsky.
Se dizolva 0,1 - 1 g polinitroderivat in 10 mL acetona si se amesteca dupa cateva minute cu 5 mL NaOH 10%. Apar coloratii specifice care se pot compara cu solutii de referinta: o-dinitrobenzenul - incolor; m-dinitrobenzenul - rosu violet; 1,2,4-trinitrobenzen - albastru intens etc.
b. Reducerea la amine aromatice.
Nitroderivatii aromatici se reduc la amine aromatice cu diverse sisteme reducatoare: Zn+HCl; Fe+HCl; Sn+HCl; SnCl2+HCl, Zn/Hg etc.
![]()
Intr-o eprubeta, cateva picaturi nitrobenzen se trateaza cu pilitura de fier si HCl conc. Dupa terminarea efervescentei, amestecul se incalzeste, la fierbere timp de 10-15 minute. Formarea anilinei se pune in evidenta prin reactia cu furfurol si acid acetic, cand se obtine o coloratie rosie.
2. Reactii de identificare a aminelor
. Bazicitatea aminelor si formarea sarurilor
Desi sunt baze slabe, aminele dau cu acizii saruri cuaternare de amoniu, ca in orice proces de neutralizare.
Proba intr-o eprubeta continand o amina alifatica sau aromatica se adauga apa si se observa solubilitatea. In continuare se adauga in picatura, o solutie de HCl 10% si se urmareste solubilizarea in apa a aminei:
R(Ar)-NH2 + HCl R(Ar)-NH3+ + Cl
Solutia se imparte in doua eprubete: in prima se adauga o picatura de AgNO3 0,01% si se observa precipitarea AgCl, iar in cealalta se introduce o solutie de NaOH 5%, cand amina insolubila separa din solutie.
Reactii de culoare datorita oxidarii aminelor.
Aminele aromatice, in special, se oxideaza cu HClO3, H2O2, PbO2 in acid acetic (reactia Lauth), cu persulfat de amoniu in prezenta AgNO3 etc. Culoarea produsilor depinde esential de natura aminei oxidate.
Cateva picaturi sau cristale de amina aromatica (anilina, benzidina etc.) se dizolva in acid acetic glacial si se adauga, fara a agita, cateva granule de dioxid de plumb (PbO2). Se observa coloratia care apare.
Reactia aminelor cu acid azotos.
Reactia de diazotare permite diferentierea aminelor aromatice primare de toate celelalte amine organice. Aminele primare alifatice formeaza cu HNO2 alcooli, iar cele aromatice saruri de diazoniu. Aminele secundare dau nitrozamine cancerigene (R1R2N-NO), iar cele tertiare nu reactioneaza.

Proba: intr-o eprubeta, se amesteca volume egale de solutie azotit de sodiu cu HCl 10%. Amestecul format se adauga, la rece (t < 5 C) peste cateva picaturi anilina. Sarea de diazoniu formata se pune in evidenta prin cuplare cu un fenol sau o alta amina aromatica, cand se formeaza coloranti azoici, rosii sau galben-portocalii.
|
REACTII PENTRU COMPUSI CARBONILICI
Metodele analitice pentru identificarea aldehidelor si cetonelor se bazeaza pe urmatoarele tipuri de reactii: (1) de culoare; (2) de aditie; (3) de condensare; (4) reactii de oxidare si reducere.
1. Reactii de culoare
a. Reactia cu fuxina decolorata (reactia Schiff).
Prepararea reactivului Schiff: 0,1 g fuxina se dizolva in 100 mL apa distilata, se adauga 1 mL HCl conc si 1 g sulfit de sodiu (Na2SO3). Dupa 20 minute solutia se decoloreaza de la sine. Reactivul se pastreaza in sticla bruna.
Proba. Intr-o eprubeta se trateaza cateva picaturi compus carbonilic cu doua picaturi de reactiv Schiff. Se observa coloratia rosie-violeta, specifica fuxinei. Prin adaugare de acid mineral culoarea trece in albastru-violet, care persista in cazul aldehidei formice si dispare repede in cazul aldehidei acetice.
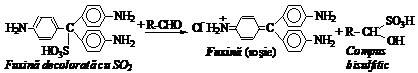
b. Reactia de culoare cu fenoli
Aldehidele condenseaza cu fenoli in prezenta H2SO4 conc formand coloranti de tip alchil-difenilmetanici intens colorati:
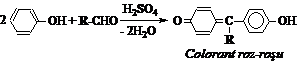
Proba: Cateva cristale rezorcina se dizolva in NaOH 50%, la usoara incalzire, se adauga cateva picaturi aldehida formica si se incalzeste la fierbere. Solutia se coloreaza de la galben la rosu.
2. Reactii de condensare
a. Condensarea aldolica si crotonica. Este o reactie comuna aldehidelor si cetonelor. In cazul aldehidei acetice, reactia se desfasoara diferentiat dupa ecuatiile:
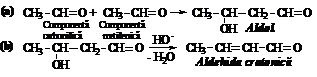
Proba: Intr-o eprubeta, peste 3 mL aldehida acetica se adauga 1 mL NaOH 10%. Se incalzeste atent pana la fierbere pe baie de apa. Apare un lichid galbui datorita formarii aldolului. Incalzind in continuare sub agitare, culoarea trece in brun si separa o masa rasinoasa care inglobeaza aldehida crotonica cu miros caracteristic, patrunzator, care poate decolora apa de brom.
b. Reactia cu fenilhidrazina. Aldehidele si cetonele dau cu fenilhidrazina substante cristalizate numite fenilhidrazone, care servesc la identificarea compusilor carbonilici.
![]()
Proba: 1 mL fenilhidrazina se trateaza, sub agitare, cu 1 mL acid acetic glacial. Rezulta acetat de fenilhidrazina, peste care se adauga cateva picaturi solutie de aldehida sau cetona. Amestecul se tine pe baia de apa 30 min si apoi se raceste. Rezulta cristale de fenilhidrazone care se filtreaza, se usuca si se determina Tt pentru a stabili natura compusului carbonilic.
Atentie! Fenilhidrazina in contact cu pielea provoaca arsuri foarte grave !
c. Reactia cu 2,4-dinitrofenilhidrazina (DNFH).
Reactivul cel mai utilizat in caracterizarea combinatiilor carbonilice este 2,4-dinitrofenilhidrazina, care conduce la dinitrofenilhildrazone de culoare galben-oranj pana la rosu inchis, cu spectre caracteristice in UV-VIS. Reactia are largi aplicatii in dozarea compusilor carbonilici prin metode colorimetrice pentru ca dinitrofenilhidrazonele se coloreaza cu alcalii.
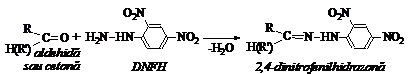
Prepararea reactivului: 0,4 g DNFH se trateaza cu 2 mL H2SO4 conc si sub agitare, cu 3mL apa distilata. La solutia calda se adauga 10 mL alcool etilic 95%.
Proba: Intr-o eprubeta se introduc 1 mL solutie 10% de compus carbonilic si 5 mL reactiv DNFH. Dupa 5-10 minute precipita 2,4-dinitrofenilhidrazona, care se filtreaza, se spala cu apa si se recristalizeaza din acetat de etil sau dioxan/apa. In final, Tt permite identificarea compusului carbonilic.
3. Reactii specifice aldehidelor
a. Autooxidarea aldehidelor se datoreaza oxigenului molecular din aer, in prezenta luminii si/sau a prooxidantilor (saruri ale metalelor grele polivalente Cu, Fe, Mn etc.) cand se formeaza peracizi care trec in acizi cu excesul de aldehida.
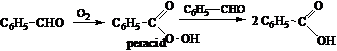
Proba: Pe o sticla de ceas se pun cateva picaturi de aldehida benzoica sau salicilica si se lasa in aer sau se sufla oxigen. Dupa 2-3 ore apar cristalele caracteristice acizilor benzoic sau salicilic.
b. Reducerea reactivilor Tollens si Fehling
b1. Solutia amoniacala de argint, [Ag(NH3)2]OH, reactiv Tollens, este redus la argint metalic de catre aldehide, care sunt oxidate la acizi.
Prepararea reactivului Tollens. Tollens I: se dizolva 1 g azotat de argint in 100 mL apa distilata si se pastreaza intr-o sticla bruna la rece. Tollens II: 10 g NaOH se dizolva in 100 mL apa distilata. Inainte de utilizare se amesteca volume egale de Tollens I cu Tollens II si se adauga in picaturi amoniac 25% pana la completa dizolvare a oxidului de argint format.
Proba: Intr-o eprubeta peste 1 mL solutie de aldehida formica se adauga 1 mL reactiv Tollens. Dupa usoara incalzire, pe baie de apa, se depune oglinda de argint.
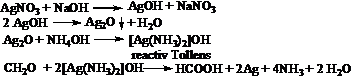
b2. Ionul cupric continut de reactivul Fehling este redus la oxid cupros de culoare rosie de catre aldehide, care se oxideaza la acizi carboxilici.
Prepararea reactivului Fehling. Fehling I: 34,6 g CuSO4 5H2O se dizolva in 500 mL apa distilata. Fehling II: 173g tartrat dublu de sodiu si potasiu (sare Seignette) si 50 g NaOH se dizolva in 500 mL apa distilata.
Intr-o eprubeta se amesteca in proportii egale reactiv Fehling I cu Fehling II cand se obtine complexul cuprotartric. Peste acest amestec se adauga cateva picaturi solutie de aldehida formica sau acetica. Se fierbe amestecul usor timp de 2 minute, apoi eprubeta se lasa in repaus cand precipita oxidul cupros de culoare rosie. Au loc reactiile:
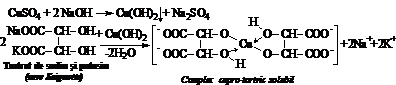
![]()
c. Reactii specifice pentru aldehida formica.
Pe langa reactiile de mai inainte, CH2O se poate identifica prin reactia cu fenilhidrazina si nitroprusiat si respectiv, fericianura.
Se trateaza 1 mL solutie ce contine CH2O cu 2-3 picaturi de solutie de clorhidrat de fenilhidrazina si 2-4 picaturi nitroprusiat 5%. Dupa alcalinizare cu NaOH 10% apare o coloratie albastra sau albastru-verde specifica.
Se trateaza 5 mL proba de CH2O cu 2-3 picaturi de solutie de clorhidrat de fenilhidrazina. Dupa 10 minute se adauga 2 picaturi fericianura de potasiu 5%, proaspat preparata. Dupa 5 minute de repaos se adauga 1 mL NaOH 30% si 1 mL izopropanol. Se agita si apare imediat o coloratie rosie.
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2025 - Toate drepturile rezervate -| |
|
|
|||
|
|||
Proiecte pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||