
| Biologie | Botanica | Chimie | Didactica | Fizica | Geografie |
| Gradinita | Literatura | Matematica |
Chimie
|
|
Qdidactic » didactica & scoala » chimie Fenolii - proprietati fizice, proprietati chimice |
Fenolii - proprietati fizice, proprietati chimice
Fenolii
Fenolii contin grupa hidroxil, legata direct cu nucleul aromatic. Ei sint denumiti dupa cel mai simplu reprezentant al clasei - fenolul. Metilfenolii sint denumiti cresoli, iar dimetilfenolii - xilenoli, derivatii de la naftalen - naftoli:
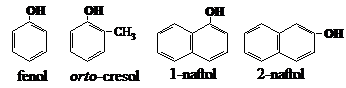
In molecula fenolilor polihidroxilici sint 2,3 sau mai multe grupe hidroxil legate de inelul benzenic:
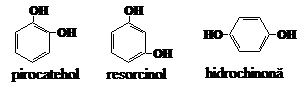
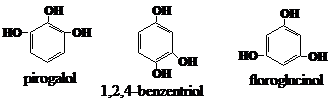
1. Proprietati fizice
Fenolii monohidroxilici sint cristalizati cu miros caracteristic, putin solubili in apa, usor solubili in alcooli si esteri. Au caracter mai polar decit alcoolii saturati corespunzatori. Temperaturile de topire si de fierbere mai ridicate ale fenolului si solubilitatea mai mare in apa fata de cele ale ciclohexanolului se datoreaza legaturilor de hidrogen mai puternice. Legatura O-H, cind nu este ionizata, este mai puternic polarizata decit la alcooli. La tratarea fenolilor cu solutie proaspata diluata de FeCl3 apare o culoare rosie-violeta pentru fenol, albastra pentru cresoli, verde pentru alti fenoli. Aparitia culorilor este rezultatul formarii unor derivati ai ionului C6H5OFe2
2. Proprietati chimice
Reactii cu participarea legaturii O-H
Fenolii au un caracter acid mai pronuntat decit alcoolii (Ka=1,7 10 10 pentru fenol dar ramin acizi mai slabi decit acidul carbonic si sulfhidric. Spre deosebire de alcooli, fenolii se dizolva in solutii apoase de baze alcaline formind fenolati. Aceasta reactie este folosita pentru a identifica fenolii si pentru a-i separa de alcooli sau acizi carboxilici:
C6H5OH NaOH C6H5ONa H2O
C6H5ONa CO2 H2O C6H5OH NaHCO3
Faptul ca fenolii sint cu caracter mai acid decit alcoolii, adica echilibrul la disociere este deplasat mai spre dreapta, se datoreaza unor efecte de conjugare: in fenolul neionizat electronii p ai oxigenului sint conjugati cu electronii p ai nucleului aromatic. Datorita acestei conjugari oxigenul se pozitiveaza si protonul poate pleca mai usor:
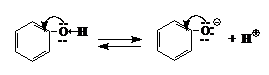
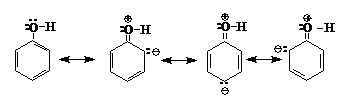
In ionul de fenolat, care rezulta la ionizarea grupei -OH, se produce o conjugare asemanatoare celei de mai sus, insa cu mult mai avansata:
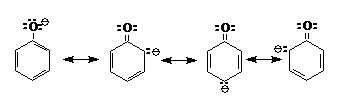
Datorita difuzarii sarcinii ionice pe intreg ciclul aromatic, sarcina este mai putin localizata pe oxigen in comparatie cu anionul alcanolat, iar tendinta ionului de fenolat de a se combina cu protonul este micsorata. Dupa cum se vede in formulele de rezonanta aratate mai sus, legatura C-OH are un oarecare caracter de dubla legatura, din care cauza grupa OH din fenol se substituie mult mai greu.
Reactiile grupei hidroxil cu ruperea legaturii O-H si formarea unei legaturi O-R sint mai dificile decit la alcooli. Astfel, se pot obtine esteri in reactie cu anhidridele acizilor sau clorurile de acil, si nu cu acizii carboxilici:
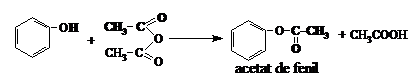
Eterii se formeaza prin tratarea fenolatilor cu derivati halogenati (metoda Williamson

Eterii metilici rezulta prin tratarea fenolatilor cu dimetilsulfat sau diazometan:
2C6H5ONa (CH3O)2SO2 2C6H5OCH3 Na2SO4
C6H5OH CH2N2 C6H5OCH3 N2
Reactii ale nucleului aromatic
Datorita grupei hidroxil, care este un substituent activant de ordinul intii, sint favorizate reactiile de substitutie electrofila in pozitiile orto si para.
Sulfonarea are loc la temperatura camerei in pozitia orto si la 100OC in pozitia para:
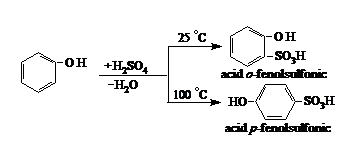
Halogenarea poate fi controlata usor cind se lucreaza in solventi anhidri:

|
Daca bromul se adauga in solutie apoasa, se formeaza 2,4,6‑tribromofenol.
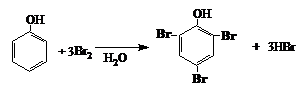
Nitrarea fenolilor are loc foarte usor cu acid azotic diluat la temperatura camerei si se obtine amestec de orto- si para-nitrofenoli:
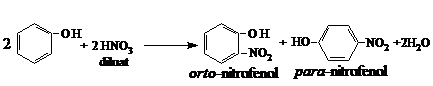
La nitrarea cu acid azotic concentrat se formeaza 2,4,6-trinitrofenol (acid picric). Nitrofenolii care se obtin sint colorati in galben deschis:
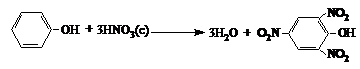
Reactii de condensare cu aldehidele. Fenolii se condenseaza foarte usor cu aldehidele. Reactia are loc ca o substitutie electrofila si poate fi catalizata de acizi si de baze.
Aldehida formica la reactie cu fenolul formeaza, mai intii, alcooli o‑hidroxibenzilic si p‑hidroxibenzilic si in continuare rasini fenoplaste:
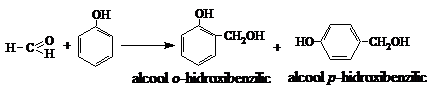
Rasini fenol-formaldehidice
In procedeele cu catalizator bazic (NaOH) fenolul si formaldehida (solutie de 40%), in raport de 1:1, la incalzire, se transforma in rezol (bachelita A), solubil in acetona. Rezolul prezinta o substanta galbena, transparenta, foarte fragila. Solutia rezolului in solventi organici este utilizata in calitate de lacuri. Prin incalzire timp de citeva minute, la 150OC, rezolul se solidifica si trece in rezita (bachelita C) cu structura reticulara tridimensionala. Aceasta are loc datorita condensarii ulterioare prin resturile -CH2OH:
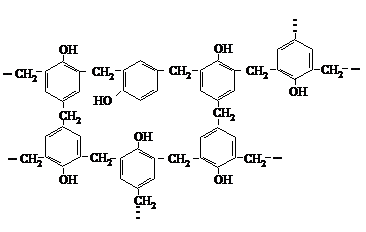
Substanta macromoleculara obtinuta are o rezistenta mecanica mare si se utilizeaza la fabricarea rotilor dintate, materialelor izolante electrice, diferitor obiecte de uz casnic etc.
In prezenta unor cantitati de acid diluat (HCl) la rece formaldehida si fenolul formeaza alcooli hidroxibenzilici, care trec cu usurinta in dihidroxidifenilmetani, iar apoi in novolacuri cu structura filiforma (masa moleculara 300 - 1300). Condensarea catalizata de acizi are loc in pozitiile orto- si para- prin intermediul carbocationului CH2OH, format la protonizarea formaldehidei:
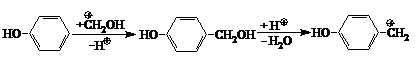
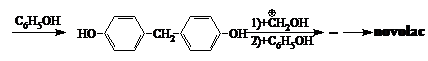
Novolacul contine macromolecule alcatuite din resturi ale fenolului unite intre ele in pozitiile orto- si para- prin intermediul gruparilor CH2
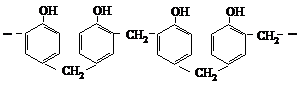
Novolacul are o structura asemanatoare cu a rezolului, insa nu contine grupe libere -CH2OH. Pentru a-l transforma in rezita el trebuie incalzit cu hexametilentetramina, care este un furnizor de grupe -CH2-. In asa mod moleculele de novolacuri se transforma in molecule reticulate tridimensionale (fenoplaste
Fenolul se condenseaza usor si cu acetona, obtinindu-se 2,2‑bis(4‑hidoxifenil)propanul, care serveste la fabricarea rasinilor epoxidice.
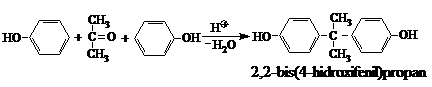
Oligomerii fenol-formaldehidici se utilizeaza larg la producerea placajului, placilor din hirtie stratificata, maselor plastice, diverselor amestecuri cu aschii sau rumegus de lemn pentru presare etc. Ele se intrebuinteaza in calitate de componenta principala a diferitor cleiuri, lacuri, ermetici etc.
Oligomerii fenol-formaldehidici se pot modifica usor prin:
policondensarea fenolului si formaldehidei in comun cu alti monomeri, cum sint, ureea, furfuralul, alcoolul butilic, colofoniu s. a.;
transformari polimer-analoage;
prin reticzlarea oligomerilor fenol-formaldehidici cu alti oligomeri sau polimeri, de exemplu oligomerii ureo-formaldehidici sau epoxidici cu poliamidele sau poliacetalii si altele.
Modificarea oligomerilor fenol-formaldehidici poate avea scopuri diferite, si anume, atribuirea unor calitati noi polimerilor si materialelor intarite, de exemplu, soliditate la soc (percutie ?), rezistenta chimica, stabilitate termica si a. In alte cazuri se imbunatatesc proprietatile liante ale cleiurilor si adezivilor obtinuti pe baza lor, si le atribuie plasticitate. Pentru atribuirea stabilitatii la actiunea uleiurilor, oligomerii destinati utilizarii in industria lacurilor si vopselelor sint modificati prin blocarea grupelor fenolice, micsorind in acest mod polaritatea lor.
Fenolii mono- si polihidroxilici nu se gasesc in natura, dar in regnul vegetal se intilnesc derivatii lor. Acestea mai au in moleculele sale in afara de grupele fenolice si alte grupe cum sint cele aldehidice, carboxilice, alcoolice etc. Multi dintre acesti fenoli se formeaza in plante, in arbori si se contin in lemn in calitate de substante extractibile. Asa sint compusii fenolici cu structura C6 - C6, C6 - C2 - C6, C6 - C3 - C6, taninurile hidrolizabile si cele condensate (vezi "Compozitia chimica a lemnului", pag. 42 - 53). Exista o legatura directa intre compusii fenolici si lignina, deoarece precursorii ligninei - alcoolii coniferilic, sinapic si cumarilic au in compozitia moleculelor sale atit grupe hidroxil alcoolice cit si fenolice (v. p. 34).
In industria de prelucrare a lemnului in afara de rasinile fenol-formaldehidice se folosesc si cele ureo- si melamin-formaldehidice.
Rasini ureo-formaldehidice
Rasinile ureo-formaldehidice se obtin prin condensarea carbamidei (ureei) cu formaldehida. Ele se produc in forma unor oligomeri, care ulterior se intaresc in prezenta catalizatorilor (intaritorilor). Insasi procesul de policondensare cel mai des se realizeaza in mediu apos. Proprietatile produselor de policondensare depind de raportul molar al substantelor initiale, de mediu de reactie (valoarea pH-ului) si temperatura.
In mediul neutru sau slab bazic (pH 7 - 8) in functie de raportul molar uree : formaldehida se pot forma de la mono- pina la tetra-derivati ai carbamidei, conform ecuatiilor:
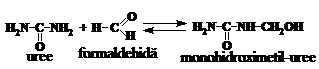

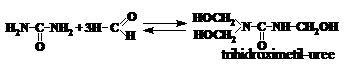
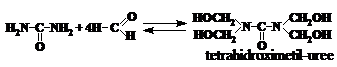
Mono- si dihidroximetil-ureele pot fi izolate din solutie sub forma de substante cristaline. Celelalte se obtin numai in solutie. In mediul puternic alcalin (pH = 11 - 13) se formeaza numai monohidroximetil-uree. In mediul puternic acid (pH = 1 - 4) se formeaza hidroximetil-uree, care deshidrateaza, formindu-se mono- si dimetilen-uree. Aceasta, la rindul sau, se transforma in polimeri insolubili, inutilizabili:
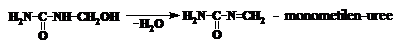
![]()
Oligomerii ureo-formaldehidici se obtin in mediul slab acid (pH = 5 - 6,5) la cald in forma de substante solubile in apa. Mecanismul reactiei de policondensare este destul de complex si poate fi prezentat:

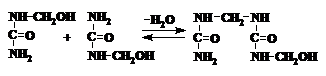
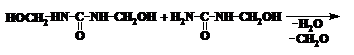
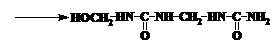
In aceste conditii de reactie monohidroximetil-ureea are reactivitate mai mare comparativ cu dihidroximetil-ureea. Insa din monohidroximetil-uree nu pot fi obtinuti polimeri cu structura ramificata sau tridimensionala cu proprietati de liant bune. La policondensarea carbamidei cu formaldehida luate in cantitati echimoleculare rezulta polimeri cu structura liniara:


La policondensarea dihidroximetil-ureei rezulta oligomeri, care in prezenta catalizatorilor acizi foarte repede, mai ales la incalzire,
![]()
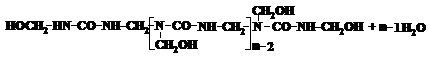
De obicei procesul de policondensare se realizeaza la valori variabile de pH: la inceput in mediu neutru sau slab bazic cu un raport molar formaldehida : carbamida de (1,5 - 2,0) : 1, iar apoi, cind se formeaza de acum o cantitate suficienta de grupe hidroximetilice (-CH2OH), in mediul slab acid acestea servesc pentru accelerarea reactiei de condensare. La prima etapa, fiind un surplus de formaldehida, se formeaza mono- si dihidroximetil-uree, care ulterior participa la policondensare, formindu-se produse cu structura liniara sau ciclica a segmentelor macromoleculei. Acestea din urma se pot intari prin policondensarea de mai departe.
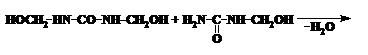
![]()
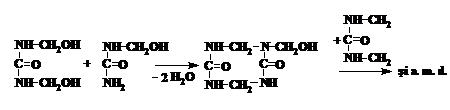
Temperatura amestecului reactant influenteaza mult reactia de policondensare a ureei cu formaldehida. De exemplu, la 60 oC se formeaza produse solubile in apa cu grad de condensare mic, care contin multa formaldehida in stare libera prin cresterea temperaturii pina la 80 - 90 oC se micsoreaza cantitatea formaldehidei libere in mediul reactant si produsele ce se formeaza se pot intari repede.
Intarirea oligomerilor ureo-formaldehidici are loc in prezenta catalizatorilor (intaritorilor) la temperatura mediului ambiant sau la incalzire si numai in cazul cind acesti oligomeri contin grupe hidroximetil libere. In calitate de catalizatori se folosesc substante cu caracter acid de natura organica (acizii oxalic, lactic) sau anorganica (acizii sulfuric, fosforic). Dar cel mai des se folosesc sarurile de amoniu ale acizilor tari: NH4Cl, (NH4)3PO4, (NH4)2SO4. Pentru cleiul in forma de pulbere se utilizeaza in calitate de catalizator clorura de zinc.
Procesul de intarire a oligomerilor ureo-formaldehidici consta in formarea legaturilor transversale intre macromolecule. Are loc interactiunea grupelor -CH2OH intre ele sau cu hidrogenul grupelor amidice -NH-. Calitatea produsului intarit este cu atit mai inalta, cu cit mai multe grupe -CH2OH sint in oligomerul initial. La intarirea oligomerilor ureo-formaldehidici au loc reactiile:
![]()
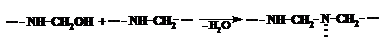
![]()
Transformarea oligomerului in polimer infuzibil si insolubil este insotita de eliminarea apei si a formaldehidei, cea ce poate fi demonstrat in modul urmator:
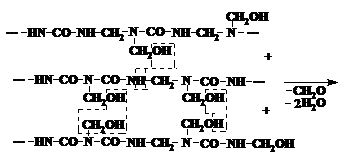
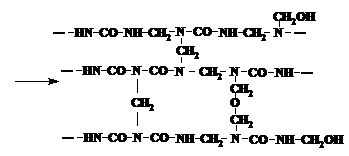
Prin deosebire de rasinile fenol-formaldehidice, cele ureo-formaldehidice chiar si dupa intarire se pot gonfla in dizolvanti si se inmoaie la incalzire. Aceasta se explica prin cantitatea mica de legaturi transversale, care apar in procesul de intarire. Densitatea acestor legaturi transversale poate spori daca se adauga in sistem intaritori speciali - substante care interactioneaza activ cu grupele functionale ale oligomerului ureo-formaldehidic. Asa sint diaminele, epoxiaminele, acetalii si a. Compozitiile ureo-formaldehidice intarite in acest mod devin mult mai rezistente la actiunea apei, asemanindu-se cu cele fenol- si melamin-formaldehidice.
Rasinile ureo-formaldehidice au intrebuintare foarte larga in industria de prelucrare a lemnului, la fabricarea placajului, placilor aglomerate din lemn, mobilei, placilor celulare din lemn, lemnului stratificat, placilor din fibre din lemn cu densitate medie, placilor aglomerate din fibre, pentru incleierea obiectelor si constructiilor din lemn. Oligomerii ureo-formaldehidici au viteza mare de intarire, iar dupa ce se intaresc nu au miros si culoare, au rezistenta buna, sint bio-rezistenti. Printre neajunsurile lor mentionam rezistenta scazuta la actiunea apei, temperaturilor inalte. Pentru ameliorarea calitatilor, polimerii ureo-formaldehidici pot fi modificati cu fenoli, melamina, amine, furfural s. a.
Rasini melamin-formaldehidice
Oligomerii melamin-formaldehidici se formeaza la condensarea melaminei cu formaldehida. Functie de raportul molar melamina : formaldehida se pot forma monohidroximetil-, dihidroximetil- si trihidroximetil-melamine:
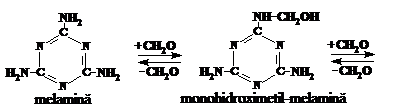

Hidroximetil-melaminele ce se obtin la I etapa condenseaza. Intre moleculele lor se formeaza legaturi dimetilen-eterice si metilenice:
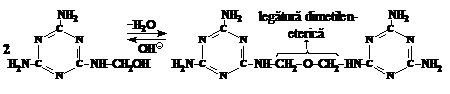
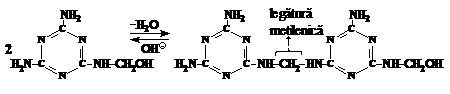
In mediu neutru sau bazic predomina formarea legaturilor dimetilen-eterice, iar in mediu acid - celor metilenice.
Oligomerii melamin-formaldehidici se intaresc prin incalzire in prezenta catalizatorilor acizi. La valori de pH = 6 - 7 ei se pot intari la temperatura de 120 - 130 oC si fara catalizatori. Oligomerii melamin-formaldehidici obtinuti dintr-un raport molar redus formaldehida : melamina gelifieaza mai repede si au rezistenta chimica inalta. Cei obtinuti dintr-un raport crescut al formaldehidei au rezistenta mecanica inalta. Grupele hidroximetilice care ramin libere, dupa intarire se pot desprinde la fierbere in apa, degajindu-se formaldehida.
Oligomerii melamin-formaldehidici in forma de solutii apoase prezinta lichide cu consistenta unui sirop si viscozitate diferita. Cel mai bine se pastreaza in timp (2 - 3 saptamini) oligomerii partial deshidratati. Dupa intarire polimerii melamin-formaldehidici sint suficient de rezistenti la actiunea apei; aceasta rezistenta este putin mai mica comparativ cu cei fenol-formaldehidici. Conform stabilitatii lor termice, polimerii melamin-formaldehidici sint din categoria medie.
La temperatura 140 - 150 oC de la molecula polimerului se desprind grupele -CH2OH, eliminindu-se formaldehida, se distrug legaturile dimetilen-eterice, trecind in legaturi metilenice, tot cu eliminarea formaldehidei. La temperaturi mai mari de 200 oC se incepe descompunerea intensiva a polimerului. Printre neajunsurile polimerilor melamin-formaldehidici mentionam pretul lor de cost inalt, stabilitatea redusa a solutiilor de incleiat, toxicitatea si rezistenta chimica nesatisfacatoare fata de unii reagenti.
Polimerii melamin-formaldehidici se utilizeaza la fabricarea compozitiilor pentru presat, materialelor plastice stratificate, placajului, placilor cu suprafete imprimate, a elementelor decorative din material fibros utilizate pentru mobila de arta. Cantitati mari se folosesc in forma de amestecuri cu oligomeri fenol-formaldehidici si ureo-formaldehidici. Polimerii melamin-formaldehidici au luciu si transparenta nobila si se utilizeaza cu succes pentru innobilarea suprafetei lemnului. In stare pura, fara a se adauga alti oligomeri, ei se utilizeaza la fabricarea aminoplastelor, la melaminarea placilor aglomerate din lemn, la impregnarea hirtiei stratului exterior de innobilare.
Pentru utilizarea in industria de producere a lacurilor si vopselelor, oligomerii melamin-formaldehidici deseori se modifica pentru ameliorarea solubilitatii lor in dizolvanti organici, capacitatii de a se amesteca cu plastifianti, cu alti oligomeri si polimeri. Rezultate bune se obtin prin cumularea oligomerilor melamin-formaldehidici cu poliesteri, uneori adaugind si oligomeri ureo-formaldehidici. Lacurile din oligomeri cumulati, care se intaresc (se usuca) la 80 - 110 oC, formeaza pelicule lucitoare, rezistente la actiunea apei si a reagentilor chimici (HCl conc., baze alcaline diluate). Peliculele rezista la temperaturi de pina la 260 oC fara asi schimba evident calitatile.
Oligomerii melamin-formaldehidici modificati pentru fabricarea lacurilor se obtin in doua trepte. La prima etapa condenseaza melamina cu formaldehida in mediu bazic, formindu-se hidroximetil-melaminele fara a se forma oligomeri. La cea de a doua treapta se produce alchilarea lor cu alcool (cel mai des alcool butilic) in mediu acid. Concomitent cu alchilarea are loc si formarea oligomerilor. Deoarece la aceasta etapa o parte din grupele hidroximetil interactioneaza cu alcoolul, iar altele participa la formarea oligomerului, se utilizeaza cel mai des penta- si hexahidroximetil-melaminele. Raportul molar al substantelor initiale - formaldehida : melamina : alcool butilic este de 8 : 1 : 8. In calitate de catalizator la a doua etapa se foloseste anhidrida ftalica (3,5 - 4 % de la masa melaminei).
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2025 - Toate drepturile rezervate -| |
|
|
|||
|
|||
Esee pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||








